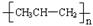1、填空题 已知 2Na2O2+2CO2=2Na2CO3+O2,因此Na2O2可在呼吸面具和潜水艇里作供氧剂。
(1)请在答卷上用双线桥法标出上述方程式的电子转移方向和数目。
(2) 是还原剂, 是还原产物。
(3)若转移3mol电子,则所产生的氧气在标准状况下的体积为 。
2、填空题 溴主要以Br-形式存在于海水中,海水呈弱碱性。工业上制备的Br2的操作步骤为:
①一定条件下,将Cl2通入浓缩的海水中,生成Br2
②利用热空气将Br2吹出,并用浓Na2CO3溶液吸收,生成NaBr、NaBrO3等
③用硫酸酸化步骤②得到的混合物
完成下列填空:
(1)Cl2氧化Br-应在 ??条件下进行,目的是为了避免?。
(2)Br2可用热空气吹出,其原因是?。
(3)写出步骤③所发生的化学反应方程式。
用硫酸而不用盐酸酸化的原因可能是 ??。步骤②的产品有时运输到目的地后再酸化,主要是因为 ?.
(4)为了除去工业Br2中微量的Cl2,可向工业Br2中?。?
a.通入HBr? b.加入Na2CO3溶液? c.加入NaBr溶液? d.加入Na2SO3溶液
3、选择题 食盐、蔗糖、醋酸、“84消毒液”、明矾等是灾后居民日常生活中经常使用的物质,下列有关说法或表示正确的是
A.食盐中阴离子的结构示意图为:
B.蔗糖和醋酸都是弱电解质
C.“84消毒液”中有效成分NaClO的电子式为: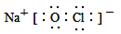
D.明矾溶液水解可制得Al(OH)3胶体,用于杀菌消毒
4、简答题 计算题
(Ⅰ)将一定质量的Fe溶于100mL4mol/L的过量稀盐酸中,完全反应后收集到H23.36L(标准状况下),若反应前后溶液的体积不变.求:
(1)被氧化的铁的质量.
(2)生成的FeCl2的物质的量浓度.
(3)反应后的溶液中H+的物质的量浓度.
(Ⅱ)在标准状况下,100mL某气体的质量是0.179克.计算这种气体的相对分子质量?
5、选择题 下列有关化学用语表示正确的是
A.中子数为20的氯原子: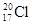
B.CO2的比例模型:
C.铝原子的结构示意图: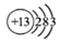
D.聚丙烯的结构简式: