1、选择题 一定量的Fe和Fe2O3混合物投入250ml 2mol/L的HNO3溶液中,反应完全后,无固体剩余,生成1.12L NO气体(标况),再向反应后溶液中加入1 mol/L的NaOH溶液,要使铁元素全部沉淀下来,所加NaOH溶液的体积最少是
A.450ml
B.500ml
C.400ml
D.无法确定
参考答案:A
本题解析:略
本题难度:一般
2、选择题 将铜粉放入稀硫酸中,加热无明显变化,但加入某盐后发现铜粉质量明显减少,则该盐不可能是
A.Fe2(SO4)3
B.NaCl
C.KNO3
D.Cu(NO3)2
参考答案:B
本题解析:金属铜可与Fe3+反应,A能;铜在酸性条件下可与硝酸根离子反应,C、D能;选B。3+ 和硝酸的氧化性。
本题难度:一般
3、填空题 某课题组研究以硫铁矿(主要成分为FeS2)为原料制备氯化铁晶体(FeCl3・6H2O)的工艺,其设计的流程如下:

回答下列问题:
(1)已知在焙烧硫铁矿石过程中铁元素转化成了Fe3O4,则该反应的化学方程式?;
(2)“酸溶”中反应的离子方程式为?;
(3)“过滤”后滤液中金属阳离子有?;
(4)“氧化”中使用的氧化剂最好是?;
(5)该工艺流程中产生的SO2会污染空气并形成酸雨,下列物质:①BaCl2②品红③石灰乳 ④O2,用于吸收SO2最好的是?。
参考答案:(1)3FeS2+8O2 Fe3O4+6SO2;(没配平扣1分,无高温不扣分。)?
Fe3O4+6SO2;(没配平扣1分,无高温不扣分。)?
(2)Fe3O4+8H+=2Fe3++Fe2++4H2O;(没配平扣1分,多写其它的离子方程式既不给分也不扣分。)
(3)Fe3+、Fe2+(各1分); (4)Cl2(H2O2等只要合理也可);(5)③
本题解析:(1)由题意可知硫铁矿中铁被氧化成了Fe3O4,可知反应式为3FeS2+8O2 Fe3O4+6SO2 ;
Fe3O4+6SO2 ;
(2)Fe3O4可溶解于盐酸中,反应的离子方程式为Fe3O4+8H+=2Fe3++Fe2++4H2O ;
(3)由Fe3O4的组成可知铁的化合价为+2和+3;
(4)氧化剂的加入是为了把其中的+2铁氧化成+3,只要不引入杂质即可,如Cl2、O3、H2O2 均可;
(5)吸收尾气SO2 工业上一般用碱性物质,如石灰乳。
本题难度:一般
4、实验题 (14分)铁、铝、铜等金属及其化合物在日常生活中应用广泛,请根据下列实验回答问题:
(1)生铁中含有一种铁碳化合物X(Fe3C)。X在足量的空气中高温煅烧,生成有磁性的固体Y,将Y溶于过量盐酸的溶液中含有的大量阳离子是________________________。
(2)某溶液中有Mg2+、Fe2+、Al3+、Cu2+等四种离子,向其中加入过量的NaOH溶液后,过滤,将滤渣高温灼烧并将灼烧后的固体投入到过量的稀盐酸中,所得溶液与原溶液相比,溶液中大量减少的阳离子是________;
A.Mg2+ B.Fe2+? C.Al3+? D.Cu2+
(3)氧化铁是重要工业颜料,用废铁屑制备它的流程如下:

回答下列问题:
①操作Ⅰ的名称是________,操作Ⅱ的名称是________。
②写出在空气中煅烧FeCO3的化学方程式?;
(4)有些同学认为KMnO4溶液滴定也能进行铁元素含量的测定(5Fe2++MnO4-+8H+===5Fe3++Mn2++4H2O)。
a.称取2.850g绿矾(FeSO4・7H2O)产品,溶解,在250mL容量瓶中定容;
b.量取25.00mL待测溶液于锥形瓶中;
c.用硫酸酸化的0.01000mol/LKMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为20.00mL。
①实验前,首先要精确配制一定物质的量浓度的KMnO4溶液250 mL,配制时需要的仪器除天平、玻璃棒、烧杯、胶头滴管外,还需_____________________________________________。
②某同学设计的下列滴定方式,最合理的是________。(夹持部分略去)(填字母序号)
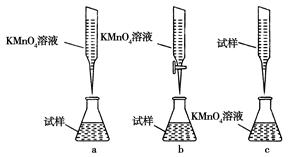
③计算上述样品中FeSO4・7H2O的质量分数为?。
参考答案:(14分)(1)Fe2+、Fe3+、H+ (2)B、C
(3)①过滤(1分) 洗涤(1分) ②4FeCO3+O2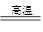 2Fe2O3+4CO2
2Fe2O3+4CO2
(4)①250 mL容量瓶 ②b ③0.975(其余均为2分)
本题解析:(1)磁性的固体Y应该是四氧化三铁,所以与足量盐酸反应后,溶液中的阳离子分别是Fe2+、Fe3+、H+。
(2)氢氧化钠是过量的,因此得不到氢氧化铝沉淀。又因为氢氧化亚铁极易被氧化生成氢氧化铁,所以滤渣应该是氢氧化铁、氢氧化镁和氢氧化铜。滤渣灼烧后生成氧化铁、氧化镁和氧化铜,与足量盐酸反应生成氯化铁、氯化镁和氯化铜,因此所得溶液与原溶液相比,溶液中大量减少的阳离子是Fe2+、Al3+,即答案选BC。
(3)①滤渣从溶液中分离出的方法是过滤,即操作I的名称是过滤。碳酸亚铁沉淀在烘干、煅烧之前必须进行洗涤,所以操作Ⅱ的名称是洗涤。
②由于亚铁离子极易被氧化,所以在空气中煅烧碳酸亚铁的的化学方程式是4FeCO3+O2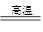 2Fe2O3+4CO2。
2Fe2O3+4CO2。
(4)①由于是配制250ml溶液,所以还需要250 mL容量瓶。
②样品的水溶液是显酸性的,应该用酸式滴定管。同样高锰酸钾溶液具有强氧化性,也应该用酸式滴定管,所以答案选b。
③根据5Fe2++MnO4-+8H+===5Fe3++Mn2++4H2O可知,25ml溶液中含有的亚铁离子的物质的量是0.01000mol/L×0.02L×5=0.001mol,则FeSO4・7H2O的质量0.001mol×278g/mol×10=2.78g,所以样品中FeSO4・7H2O的质量分数为2.78g÷2.850g=0.975,即97.5%。
本题难度:一般
5、填空题 【化学一选修2:化学与技术】(15分)
利用硫酸工业废渣(主要含Fe2O3、SiO2、Al2O3、MgO等杂质)制备氧化铁的工艺流程如下:
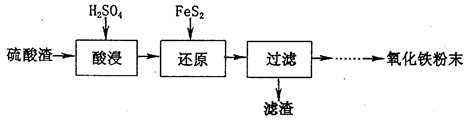
(1)“酸浸”中硫酸要适当过量,目的是:①提高铁的浸出率,②__________________。
(2)“还原”是将Fe3+转化为Fe2+,同时FeS2被氧化为SO ,该反应的离子方程式为____________.
,该反应的离子方程式为____________.
(3)为测定“酸浸”步骤后溶液中Fe3+的量以控制加入FeS2的量。
实验步骤为:准确量取一定体积的酸浸后的溶液于锥形瓶中,加入HCl、稍过量SnCl2,再加HgCl2除去过量的SnCl2,以二苯胺磺酸钠为指示剂,用K2Cr2O7标准溶液滴定,有关反应方程式如下:
2Fe3++Sn2++6Cl-===2Fe2++SnCl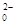
Sn2++4Cl-+2HgCl2="==" SnCl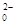 +Hg2Cl2↓
+Hg2Cl2↓
6Fe2++ Cr2O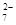 +14H+===6Fe3++2Cr3++7H2O
+14H+===6Fe3++2Cr3++7H2O
①若SnCl2不足量,则测定的Fe3+量__________(填“偏高”、“偏低”、“不变”,下同)。
②若不加HgCl2,则测定的Fe3+量偏高,其原因是_____________。
(4)①可选用______________(填试剂)检验滤液中含有Fe3+。产生Fe3+的原因是_________________(用离子反应方程式表示)。
②已知部分阳离子以氢氧化物形式沉淀时溶液的,pH见下表:
沉淀物
| Fe(OH)3
| Fe(OH)2
| Al(OH)3
| Mg(OH)2
| Mn(OH)2
|
开始沉淀
| 2.3
| 7.5
| 3.4
| 9.4
| 8.3
|
完全沉淀
| 3.2
| 9.7
| 4.4
| 12.4
| 9.8
|
实验可选用的试剂有:稀HNO3、Ba(NO3)2溶液、酸性KMnO4溶液、NaOH溶液,要求制备过程中不产生有毒气体。请完成由“过滤”后的溶液模拟制备氧化铁的实验步骤:
a.氧化:________________________________;b.沉淀:_____________________________;
c.分离,洗涤;d.烘干,研磨。
参考答案:(1)抑制Fe3+的水解(2分)
(2)14Fe3++FeS2+8H2O ===15Fe2++2SO +16H+(2分)
+16H+(2分)
(3)①偏低,②若不加HgCl2,溶液中含有Sn2+,也可以被酸性高锰酸钾氧化,消耗的酸性高锰酸钾氧化偏大,则测定的Fe3+量偏高。(2分)
(4)①KSCN(2分);4Fe2++O2+4H+ ===4Fe3++H2O (2分);
②a.向溶液中加入过量的酸性高锰酸钾溶液,搅拌(2分);
b.滴加NaOH溶液,调节溶液的pH为3.2~3.8(2分)
本题解析:(1) 酸浸”中硫酸要适当过量,抑制Fe3+的水解;
(2)由信息Fe3+转化为Fe2+,同时FeS2被氧化为SO ,在利用氧化还原反应配平方程式:14Fe3++FeS2+8H2O ===15Fe2++2SO
,在利用氧化还原反应配平方程式:14Fe3++FeS2+8H2O ===15Fe2++2SO +16H+;
+16H+;
(3)①若SnCl2不足量,Fe3+没有完全还原为Fe2+,则测定的Fe3+量偏低,②若不加HgCl2,溶液中含有Sn2+,也可以被酸性高锰酸钾氧化,消耗的酸性高锰酸钾氧化偏大,则测定的Fe3+量偏高。
(4)①检验滤液中含有Fe3+是KSCN溶液;Fe2+的氧化反应是:4Fe2++O2+4H+ ===4Fe3++H2O;
②a.向溶液中加入过量的酸性高锰酸钾溶液,搅拌;b.滴加NaOH溶液,调节溶液的pH为3.2~3.8,使Fe3++完全沉淀。
本题难度:困难