1、选择题 稀溶液中,氧化性HClO>H2SO4;在25℃时,电离常数:K1(H2CO3)>K(HClO)>K2(H2CO3).则以下离子方程式错误的是
A.CO2?通入饱和Na2CO3溶液中CO2+2Na++CO32-+H2O═2NaHCO3↓
B.少量CO2通入次氯酸钙溶液中?CO2+H2O+ClO-═HCO3-+HClO
C.少量SO2通入次氯酸钙溶液中?Ca2++2ClO-+SO2+H2O═CaSO3↓+2HClO
D.过量CO2通入澄清石灰水中?CO2+OH-═HCO3-
参考答案:C
本题解析:分析:由电离平衡常数可知,K越大,酸性越强,以此分析A、B、D,由氧化性HClO>H2SO4可知,选项C中应发生氧化还原反应,以此来解答.
解答:A.由K1(H2CO3)>K2(H2CO3),则CO2?通入饱和Na2CO3溶液中的离子反应为CO2+2Na++CO32-+H2O═2NaHCO3↓,故A正确;
B.由K1(H2CO3)>K(HClO),少量CO2通入次氯酸钙溶液中的离子反应为CO2+H2O+ClO-═HCO3-+HClO,故B正确;
C.由氧化性HClO>H2SO4可知,少量SO2通入次氯酸钙溶液中的离子反应为Ca2++ClO-+SO2+H2O═CaSO4↓+2H++Cl-,故C错误;
D.由K1(H2CO3)>K2(H2CO3),过量CO2通入澄清石灰水中的离子反应为CO2+OH-═HCO3-,故D正确;
故选C.
点评:本题考查离子反应方程式书写的正误判断,注意信息中的电离常数与氧化性强弱的应用是解答本题的关键,明确强酸制取弱酸及发生的氧化还原即可解答,题目难度中等.
本题难度:一般
2、选择题 物质的量浓度相同的下列溶液,pH由大到小排列正确的是
[? ]
A.Ba(OH)2、Na2SO3、FeCl3、KCl
B.Na2SiO3、Na2SO3、KNO3、NH4Cl
C.NH3·H2O、H3PO4、Na2SO4、H2SO4
D.NaHCO3、CH3COOH、C2H5OH、HCl
参考答案:B
本题解析:
本题难度:一般
3、选择题 几位同学在一起讨论问题,你认为正确的是(?)
A.水溶液中有离子参加的反应就是离子反应
B.离子反应是指在水溶液中进行的反应
C.参加离子反应的物质必须都是电解质
D.凡是没有沉淀、气体和水生成的反应都不是离子反应
参考答案:A
本题解析:有离子参加的反应就是离子反应,并不一定在水溶液进行,故A项正确,B项错误;参加离子反应的物质不一定都是电解质,如单质与离子的反应,也是离子反应,故C项错误;有沉淀、气体和水生成的反应只是复分解反应这一类离子反应的条件,对于单质与离子间的置换反应类的反应就不符合,故D项错误。
本题难度:简单
4、填空题 弱电解质的电离平衡、盐类的水解平衡和难溶物的溶液平衡均属于化学平衡。
I、已知H2A在水中存在以下平衡:H2A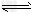 H++HA-,HA-
H++HA-,HA- H++A2-。
H++A2-。
(1)NaHA溶液的pH______(填大于、小于或等于)?Na2A溶液的pH。
(2)某温度下,若向0.1?mol/L的NaHA溶液中逐滴滴加0.1?mol/L?KOH溶液至溶液呈中性。此时该混合溶液中下列关系中,一定正确的是_____________。
a.c(H+)·c(OH-)=1×10-14?
b.c(Na+)+c(K+)=c(HA-)+2c(A2-)
c.c(Na+)>c(K+)?
d.c(Na+)+c(K+)=0.05?mol/L
(3)已知常温下H2A的钙盐(CaA)饱和溶液中存在以下平衡:CaA(s) Ca2+(aq)+A2-(aq)?△H>0。
Ca2+(aq)+A2-(aq)?△H>0。
①降低温度时,Ksp______?(填“增大”、“减小”或“不变”)。
②滴加少量浓盐酸,c(Ca2+)?____________(填“增大”、“减小”或“不变”)。
II、含有Cr2O72-的废水毒性较大,某工厂废水中含5.00×10-3?mol/L的Cr2O72-。为使废水能达标排放,作如下处理:
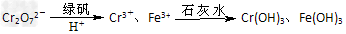
(4)该废水中加入绿矾和H+,发生反应的离子方程式为:__________________。
(5)欲使10L该废水中的Cr2O72-完全转化为Cr3+,理论上需要加入_______g?FeSO4·7H2O。
(6)若处理后的废水中残留的c(Fe3+)=2×10-13mol/L,则残留的Cr3+的浓度为____________。(已知:Ksp[Fe(OH)3]=4.0×10-38?Ksp[Cr(OH)3]=6.0×10-31)
参考答案:(1)小于
(2)bc
(3)①减小;②增大?
(4)Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O
(5)83.4g
(6)3×10-6mol/L
本题解析:
本题难度:一般
5、选择题 下列物质中,属于电解质的是
A.CO2
B.Na
C.BaSO4
D.NaOH溶液
参考答案:BC
本题解析:电解质是指在水溶液中或熔融状态下能够导电的化合物。题目中只有B和C是符合条件的,其中HCl在水溶液中可以导电,BaSO4在熔融状态下可以导电。NaOH溶液是混合物;CO2通入水中虽可以导电,但原因是生成了H2CO3,H2CO3是电解质。?
本题难度:简单