1、选择题 设NA为阿伏加德罗常数的数值,下列说法中正确的是(?)
A.标准状况下,22.4L Cl2完全溶于水时,转移电子数为NA
B.常温下, pH=l的H2SO4溶液中含有的H+的数目为0.2NA
C.标准状况下,2.24 L NH3中含有共价键的数目为NA
D.常温下,23 g NO2和N2O4的混合气体中含有NA个氧原子
参考答案:D
本题解析:A氯气溶于水时只有很少一部分氯气和水反应,产生盐酸和次氯酸。所以转移电子数小于NA。错误。B.常温下, pH=l的H2SO4溶液中含有的H+的浓度是0.1mol/L.但由于缺体积,所以无法计算H+的数目。错误。C.每个NH3中含有三个共价键。标准状况下,2.24 L NH3中含有共价键的数目为0.3NA.错误。D.NO2的相对原子质量是46.23 g NO2含有的电子数0.5mol×2NA.=NA;N2O4的相对原子质量是92,23 g N2O4含有的电子数0.25mol×4NA=NA。故23 g NO2和N2O4的混合气体中含有NA个氧原子。正确。
本题难度:一般
2、选择题 在标准状况下,560ml某气体的质量为1.1g,这种气体可能是(?)
A? CO? B? N2? C? CO2? D? N2O
参考答案:CD
本题解析:根据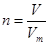 可知,标准状况下,560ml气体的物质的量是
可知,标准状况下,560ml气体的物质的量是
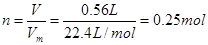 。根据
。根据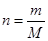 可知,该物质的相对分子质量是1.1÷0.25=44,所以根据化学式可判断,选项CD是正确的,AB的相对分子质量都是28,答案选BD。
可知,该物质的相对分子质量是1.1÷0.25=44,所以根据化学式可判断,选项CD是正确的,AB的相对分子质量都是28,答案选BD。
本题难度:简单
3、计算题 将6.5g锌放入足量的稀硫酸中充分反应,得到80mL混合溶液。试计算:
(1)反应完全后,生成标准状况下的H2多少L?
(2)所得溶液中硫酸锌的物质的量浓度是多少?
参考答案:(1)2.24L;(2)1.25mol・L-1
本题解析:略
本题难度:一般
4、实验题 实验室需用CuSO4・5H2O体配制480mL0.1mol/L的CuSO4溶液,请回答下列问题:
(1)应用托盘天平称取CuSO4・5H2O晶体_______g。
(2)若在称量样品时,药品放在天平右盘上,砝码放在天平左盘上(1g以下使用游码),天平平衡时,实际称量的CuSO4・5H2O晶体是__________g。
(3)本实验用到的主要仪器有:托盘天平、量筒、烧杯、玻璃棒、________、________。
(4)配制过程中有几个关键的步骤和操作如下图所示:将这些实验步骤A―F按实验过程先后次序排
列 。
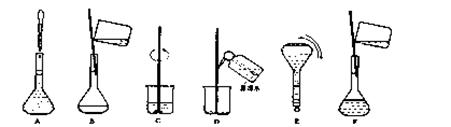
其中定容的具体操作是 。
(5)以下情况会使所配溶液的浓度产生何种影响(A.偏高 B.偏低 C.不变,填序号。):
①溶解晶体用的烧杯和玻璃棒未洗涤:____________;
②定容时俯视刻度线:____________;
③所用CuSO4・5H2O晶体已失去部分结晶水:____________。
参考答案:(1)12.5 (2)11.5 (3)500ml容量瓶 胶头滴管
(4)CBDFAE 其中定容的具体操作是:向容量瓶中加入蒸馏水,到液面离刻度线1~2cm处时,改用胶头滴管加蒸馏水至凹液面最低点与刻度线相切 (5)B;A;A
本题解析:(1)配制溶液的体积为480ml,而容量瓶的规格没有480ml,只能选用500ml容量瓶。因此需要CuSO4的物质的量n=cV=0.5L×0.1mol?L-1=0.05mol。CuSO4?5H2O的物质的量等于CuSO4的物质的量,所以CuSO4?5H2O的质量=0.05mol×250g/mol=12.5g。
(2)若药品与砝码放反,根据天平平衡原理m(左盘)=m(右盘)+游码读数,故实际称量硫酸铜晶体的质量为12g-0.5g=11.5g。
(3)溶液配制一般步骤是:计算→称量→溶解、冷却→移液→洗涤→定容→摇匀→装瓶贴签,一般用天平称量(用到药匙)固体,在烧杯中溶解,并用玻璃棒搅拌,冷却后转移到500mL容量瓶中,并用玻璃棒引流,转移完毕,用少量蒸馏水洗涤烧杯及玻璃棒2~3次并将洗涤液全部转移到容量瓶中,再加适量蒸馏水,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,使溶液的凹液面的最低点与刻线相平,塞好瓶塞,反复上下颠倒摇匀。所以需要的仪器为:托盘天平、药匙、烧杯、玻璃棒、500mL容量瓶、胶头滴管,因此还需要的仪器为:500mL容量瓶、药匙、胶头滴管。
(4)由(3)中溶液配制的一般步骤可知,正确的操作顺序为:CBDFAE。其中定容的具体操作是:向容量瓶中加入蒸馏水,到液面离刻度线1~2cm处时,改用胶头滴管加蒸馏水至凹液面最低点与刻度线相切。
(5)①溶解晶体用的烧杯和玻璃棒未洗涤,少量硫酸铜沾在烧杯壁与玻璃棒上,移入容量瓶内硫酸铜的物质的量减少,所配溶液的浓度偏低,故答案为:B。
②定容时俯视刻度线,液面在刻度线下方,溶液的体积偏小,所配溶液的浓度偏高,故答案为:A。
③所用CuSO4?5H2O晶体已失去部分结晶水,硫酸铜的质量分数增大,实际称量的硫酸铜晶体中硫酸铜的质量偏大,所配溶液的浓度偏,答案选A。
考点:考查硫酸铜溶液的配制、仪器选择、固体称量等基本实验操作以及误差分析等
本题难度:一般
5、选择题 300?mL?Al2(SO4)3溶液中,含Al3+为1.62?g,在该溶液中加入0.1?mol/L?Ba(OH)2溶液300?mL,反应后溶液中SO42-的物质的量浓度为
[? ]
A.0.4?mol/L?
B.0.3?mol/L
C.0.2?mol/L?
D.0.1?mol/L
参考答案:D
本题解析:
本题难度:简单