| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学试题《化学反应速率》试题强化练习(2019年最新版)(六)
参考答案:D 本题解析:A、分离沸点相差较大的互溶液体混合物用蒸馏的方法,温度计水银球应位于蒸馏烧瓶支管口处,错误;B、研究不同催化剂对反应速率的影响应保证H2O2的浓度相同,错误;C、图③形成原电池,电流计的指针发生偏转,错误;D、对反应: 本题难度:一般 4、填空题 (7分)环境中氮氧化物的合理控制和治理是减少雾霾天气、优化生存环境的有效途径之一。请运用化学反应原理知识,回答下列问题: |
参考答案:(7分)
(1)CH4(g) + 2NO2(g) = N2(g) +CO2(g) + 2H2O(l) △H = ―956.5kJ?mol?1(2分)
(2)①0.006mol?(L?min)-1(2分,没写单位或错误0分)
② C、D (2分)③ 增大 (1分)
本题解析:(1)首先写出CH4将NO2还原为N2的化学方程式并注明状态,CH4(g) + 2NO2(g) = N2(g) +CO2(g) + 2H2O(l),然后根据盖斯定律可得△H =1/2△H1 +1/2△H2=―956.5kJ?mol?1,进而得出热化学方程式。
(2)①根据C(s)+2NO(g)  N2 (g)+CO2 (g),生成N2的物质的量为0.09mol,则反应的NO为0.18mol,所以v(NO)=△c(NO)/△t=0.18mol÷3L÷10min=0.006mol?(L?min)-1。
N2 (g)+CO2 (g),生成N2的物质的量为0.09mol,则反应的NO为0.18mol,所以v(NO)=△c(NO)/△t=0.18mol÷3L÷10min=0.006mol?(L?min)-1。
②该反应气体系数前后相等,所以容器内压强为定值,容器内压强保持不变不能说明反应达到平衡,错误;B、速率关系为v(NO)(正) ="2" v (N2)(逆)时,表示正反应速率等于逆反应速率,反应达到平衡,错误;C、容器内气体的体积分数不变时,说明正反应速率等于逆反应速率,反应达到平衡,正确;D、该反应进行时,气体的质量发生变化,气体的物质的量发生变化,等于密度变化,则混合气体的密度保持不变时,反应达到平衡,正确。
③在容器中放入生石灰,CaO与CO2反应,CO2的浓度减小,平衡向正反应方向移动,则NO的平衡转化率增大。
考点:本题考查热化学方程式的书写、化学反应速率、化学平衡。
本题难度:困难
5、填空题 (16分)
Ⅰ.可逆反应:A(g)+3B(g) 2C(g)+3D(g),取1 mol A和2 mol B置于2L容器内。1分钟后,测得容器内A的浓度为0.2 mol/L。
2C(g)+3D(g),取1 mol A和2 mol B置于2L容器内。1分钟后,测得容器内A的浓度为0.2 mol/L。
(1)这时B的浓度为________mol/L,C的浓度为________mol/L。
(2)这段时间内反应的平均速率若以D的浓度变化来表示,应为________mol/(L・min)。
(3)如果保持容器内温度不变,反应前和反应后容器内压强之比为_____(最简整数比)。
Ⅱ.电解原理在化学工业中有广泛应用。下图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液。请回答以下问题: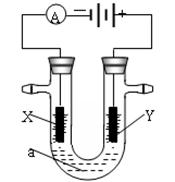
(4)在X极附近观察到的实验现象是:放出气体且______________。检验Y电极反应产物的方法是:把__________________放在Y电极附近,试纸变蓝色。
(5)当通过电解池通过1 mol电子时,两极共收集到________L气体(标准状况),电解池内的液体稀释到500 mL时,NaOH溶液浓度为________mol/L。
参考答案:(16分,每空2分,不写单位得0分。)
(1)0.1 mol/L? 0.6 mol/L
(2)0.9 mol/(L・min)
(3)5:6
(4)溶液变红?湿润的碘化钾淀粉试纸(不答湿润不给分)
(5)22.4? 2
本题解析:略
本题难度:简单
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学知识点总结《物质的量》.. | |