|
�߿���ѧ���⡶��ѧ��Ӧ���ʡ�����ǿ����ϰ��2019�����°棩(��)
2019-07-04 01:58:56
�� �� �� ��
|
1��ѡ���� �����ܱ������У�ij��Ӧ�Ļ�ѧ��Ӧ������ʱ��仯��ϵ��ͼ��ʾ������˵�������ϸ�ͼʾ���ǣ�������
A���ﵽƽ��ʱ�����淴Ӧ�������
B������Ӧ���Ũ�ȣ���Ӧ��ƽ��I�仯��ƽ��II
C����Ӧ�ﵽƽ��I�Ժ�С��Ӧ��Ũ�ȣ�ƽ���ƶ���II
D����Ӧ�ﵽƽ��IIʱ�Ļ�ѧ��Ӧ���ʱ�ƽ��Iʱ�Ĵ�
| 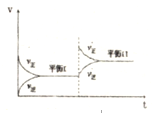
�ο��𰸣�A�������淴Ӧ�������ʱ�������ʵ�Ũ�Ȳ��䣬�ﵽƽ��״̬����A��ȷ��
B����ƽ���Ļ���������Ӧ���������淴Ӧ������ԭ��������������������Ӧ���ʴ����淴Ӧ���ʣ�ӦΪ����Ӧ���Ũ�ȣ���B��ȷ��
C���練Ӧ���С�������淴Ӧ���ʶ���С�����淴Ӧ���ʴ�������Ӧ���ʣ���C����
D����ͼ���֪��������Ϊ��Ӧ���ʣ���Ӧ�ﵽƽ��IIʱ�Ļ�ѧ��Ӧ���ʱ�ƽ��Iʱ�Ĵ�D��ȷ��
��ѡC��
���������
�����Ѷȣ���
2������� A��B��Ӧ����C���ٶ���Ӧ��A��B��ʼ�����ǵ���ʼŨ�Ⱦ�Ϊ1 mol��L��1����Ӧ����2min��A��Ũ��Ϊ0.8 mol��L��1? ,B��Ũ��Ϊ0.6 mol��L��1 C��Ũ��Ϊ0.6 mol��L��1
��1��2min�ڷ�Ӧ��ƽ����Ӧ����Ϊ�� ��(A)=??
��2����(A)����(B)����(C) ����֮��Ĺ�ϵ�ǣ�?
��3���÷�Ӧ�Ļ�ѧ��Ӧ����ʽ��?
�ο��𰸣���1����(A)��0.1 mol�qL��1min-1��2����(A)����(B)����(C)=1��2��3��3��A+2B��3C
����������������⣬��Ӧ���е�2minʱA��B��Ũ�ȷֱ������0.2mol/L��0.4mol/L��ͬʱ������0.6mol/L������ݱ仯��֮������Ӧ�Ļ�ѧ������֮�ȿ�֪���÷�Ӧ�ķ���ʽ��A+2B��3C������2min�ڷ�Ӧ��ƽ����Ӧ����Ϊ��(A)��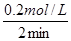 ��0.1 mol�qL��1min-1����Ϊ��Ӧ����֮������Ӧ�Ļ�ѧ������֮�ȣ����Ԧ�(A)����(B)����(C) ����֮��Ĺ�ϵ�Ǧ�(A)����(B)����(C)=1��2��3�� ��0.1 mol�qL��1min-1����Ϊ��Ӧ����֮������Ӧ�Ļ�ѧ������֮�ȣ����Ԧ�(A)����(B)����(C) ����֮��Ĺ�ϵ�Ǧ�(A)����(B)����(C)=1��2��3��
�����������ǻ���������Ŀ��飬��Ҫ�ǿ���ѧ���Է�Ӧ���ʺ��塢�����Լ���Ӧ���ʺͻ�ѧ��������ϵ���˽����������ּ�ڹ���ѧ���Ļ��������ѧ����Ӧ��������ѧϰЧ�ʡ�
�����Ѷȣ�һ��
3��ѡ���� ���������µķ�Ӧ���ų�H2�����ǣ���������
| ��������ĩ״��/mol | ���Ũ�Ⱥ������mL�� | ��Ӧ�¶�
��
Mg
0.1
3mol/LH2SO4
10
20��
��
Al
0.1
3mol/LHCl
10
20��
��
Zn
0.1
?3mol/LCH3COOH
10
20��
��
Fe
0.1
6mol/LHNO3
10
20��
|
A����
B����
C����
D����
�ο��𰸣��������ѧ���ʵ������Ƿ�Ӧ�ﱾ�������ʣ�������������þ�Ļ�������ǿ���������ᷴӦ�ı������������ӷ�Ӧ��3mol/LH2SO4�������ӵ�Ũ��Ϊ6mol/L��3mol/LHCl�������ӵ�Ũ��Ϊ3mol/L��3mol/LCH3COOH�������ӵ�Ũ��ΪԶС��3mol/L��6mol/LHNO3�������ӵ�Ũ��Ϊ6mol/L���������������Ӧ�ò�����������ѡ��A��
���������
�����Ѷȣ���
4������� ��һ���������ܱ������м���2mol?A��0.6mol?C��һ������B�������壮һ�������·�����Ӧ��������Ũ����ʱ��仯��ͼһ��ʾ��ͼ��Ϊt2ʱ�̺�ı䷴Ӧ������ƽ����ϵ�з�Ӧ������ʱ��仯����������ĸ��ζ����ı�һ�ֲ�ͬ����������֪t3��t4��ʹ���˴�����ͼһ��t0��t1��c��B��δ������
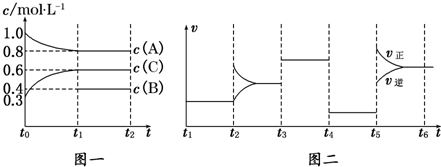
��1����t1=15min����t0��t1����CŨ�ȱ仯��ʾ�ķ�Ӧ����Ϊv��C��=______��
��2��t4��t5�θı������Ϊ______��B����ʼ���ʵ���Ϊ______��
��3���ж�ͼһ�п��淴Ӧ�ﵽƽ��״̬�������ǣ�����ţ�______��
��2v����A��=3v�棨C��
�ڻ��������ܶȲ���
�ۻ�������ƽ����Է�����������
��A��B��C��Ũ�ȶ����ٷ����仯
��4��t5��t6�α����������¶Ȳ��䣬��A�����ʵ������仯��0.01mol�����˹����������������Ƚ�������Ϊa?kJ��д�����¶��¸÷�Ӧ���Ȼ�ѧ����ʽ��______��
��5������ͬ�����£�����ʼʱ�����м���a?mol?A��b?mol?B��c?mol?C��Ҫ�ﵽt1ʱ��ͬ����ƽ�⣬a��b��cҪ���������Ϊ______��
�ο��𰸣���1��v=��c��t=0.6mol/L-0.3mol/L15min=0.02?mol/��L?min�����ʴ�Ϊ��0.02?mol/��L?min����
��2�����ͼһ��֪��A�ı仯Ϊ0.2mol/L��C�ı仯��Ϊ0.3mol/L����ѧ��Ӧ������֮�ȵ��ڻ�ѧ����ʽǰ�ļ���ϵ���ȣ�
��д���÷�Ӧ�ķ���ʽΪ2A��g��+B��g��

3C��g����ѹǿ��С�����淴Ӧ���ʼ�С��Ӧ��Ӧǰ������Ļ�ѧ������֮����ȣ���ı�ѹǿƽ�ⲻ�ƶ�������t4��t5�θı������Ϊ��Сѹǿ��
B��ƽ��Ũ����0.4mol/L�����ݷ���ʽ��֪��Ũ�ȵĸı�ֵ�뻯ѧ�����������ȣ�C�ı�0.3mol/L����B�ı�0.1mol/L��
������ʼʱӦΪ0.5mol/L����ʼ2molA����Ӧ��Ũ��Ϊ1mol/L�������Ӧ��2L��
����B����ʼ���ʵ���Ϊ0.5mol/L��2L=1mol��
�ʴ�Ϊ����Сѹǿ��?1.0?mol��
��3���ٷ�Ӧ��ƽ��״̬ʱ�����淴Ӧ������ȣ�����3v����A��=2v�棨C�����ʢٴ���
����������������䣬������������䣬��Ӧ�����Ƿ�ﵽƽ��״̬���ܶȶ����䣬������Ϊ�ж��Ƿ�ﵽƽ������ݣ��ʢڴ���
�۷�Ӧǰ����������ʵ������䣬�������䣬��������ƽ����Է����������䣬������Ϊ�ж��Ƿ�ﵽƽ������ݣ��ʢ۴���
�ܵ��ﵽƽ��״̬ʱ��A��B��C��Ũ�ȶ����ٷ����仯������Ϊƽ��״̬���ж����ݣ��ʢ���ȷ��
�ʴ�Ϊ���ܣ�
��4�����ݷ���ʽ���㣬��A�����ʵ������仯��0.01mol�����˹����������������Ƚ�������Ϊa?kJ����Ӧ2molAʱ����������200akJ������ͼ���֪��t5��t6��ӦΪ�����¶ȣ�����Ӧ���ʴ����淴Ӧ���ʣ�ƽ��������Ӧ�����ƶ���������ӦΪ���ȷ�Ӧ�������Ȼ�ѧ����ʽΪ2A��g��+B��g��?

?3C��g����H=+200a?kJ/mol��
�ʴ�Ϊ��2A��g��+B��g��?

?3C��g����H=+200a?kJ/mol��
��5����Ӧ�ķ���ʽΪ2A��g��+B��g��?

?3C��g����
���ݷ���ʽ���㣬��ʼʱ����C��������ת��ΪA��B��
��A�����ʵ���Ϊ2mol+23��0.6mol=2.4mol��B�����ʵ���Ϊ1mol+13��0.6mol=1.2mol��
����ͬ�����£�����ʼʱ�����м���a?mol?A��b?mol?B��c?mol?C��Ҫ�ﵽt1ʱ��ͬ����ƽ�⣬���������ʵ����ʵ��������������ԭƽ����ȣ�
������a+2c3=2.4��b+c3=1.2��
�ʴ�Ϊ��a+2c3=2.4��b+c3=1.2��
���������
�����Ѷȣ�һ��
5��ѡ���� �������и�����Һ��
��10��ʱ10 mL 0.1 mol��L��1��Na2S2O3��Һ��50 mL0.05 mol��L��1��H2SO4��Һ��
��10��ʱ10 mL 0.05 mol��L��1��Na2S2O3��Һ��10 mL 0.1 mol��L��1��H2SO4��Һ��
��30��ʱ10 mL 0.05 mol��L��1��Na2S2O3��Һ��10 mL 0.1 mol��L��1��H2SO4��Һ��
��ͬʱ�����ǻ�Ϸ�����Ӧ��Na2S2O3��H2SO4=Na2SO4��S����SO2����H2O������ֻ��ǵ��Ⱥ�˳���ǣ�?��
A���٢ڢ�
B���ڢ٢�
C���ۢڢ�
D���٢ۢ�
�ο��𰸣�C
����������¶�Խ�ߣ���Ӧ����Խ�죬�۵ķ�Ӧ���������ͬ�¶��£��ڻ��Һ��Na2S2O3��H2SO4��Ũ�ȴ��ڢ٣��ʷ�Ӧ���ʢ�>�١�
�����Ѷȣ�һ��
| 