1、选择题 室温下向10 mL c(H+)=10-3 mol・L-1的醋酸溶液中加水稀释后,下列说法正确的是
A.溶液中导电粒子的数目减少
B.溶液中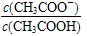 变大
变大
C.醋酸的电离程度增大,c(OH-)亦增大
D.再加入10 mL c(OH-)=10-3 mol・L-1的NaOH溶液,醋酸与NaOH恰好完全反应
2、选择题 用蒸馏水逐步稀释0.2 mol/L的稀氨水时,若温度不变,在稀释过程下列数据始终保持增大趋势的是( )
A.c(OH-)
B.c(NH4+)
C.c(NH3・H2O)
D.c(NH4+)/c(NH3・H2O)
3、选择题 物质的量浓度相同的下列溶液:HCl、H2SO4、CH3COOH,导电能力由强到弱的顺序是
[? ]
A.HCl=H2SO4>CH3COOH
B.H2SO4>HCl>CH3COOH
C.HCl>H2SO4>CH3COOH
D.HCl=H2SO4=CH3COOH
4、填空题 ( 10分)下列物质:①NaCl固体②无水乙醇③稀硫酸④BaSO4固体⑤冰醋酸⑥H2⑦CO2⑧熔融的KOH(选序号填空)
(1)能导电:_____________(2)非电解质:_____________________
(3)强电解质:_____________(4)弱电解质:____________________
(5)已知25℃时两种酸的电离常数:
Ka(CH3COOH)=1.75×10-5, Ka(HClO)=3.0×10-8
判断该反应是否能发生,若能,完成反应方程式;若不能,无需。
CH3COOH +? Ca(ClO)2? ――
5、选择题 在H2O+CH3COO-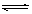 ?CH3COOH + OH―的平衡中,要使水解平衡向右移动,应采取的措施是
?CH3COOH + OH―的平衡中,要使水解平衡向右移动,应采取的措施是

A.加入NaOH固体
B.加入冰醋酸
C.增大压强
D.升高温度