1、填空题 根据组成原电池的条件,试以反应:Fe+Cu2+=Fe2++Cu设计一个原电池,画出示意图并标出原电池的正、负极和电子的流向(画在下面方框中),写出电极反应式。
供选用的电解质溶液有:稀硫酸、硫酸铜溶液、氯化铜溶液。
供选用的电极材料有:锌片、铜片、铁片、石墨。
电极材料及电极反应式:
负极材料:?,电极反应式:??
正极材料:?,电极反应式:??
电解质溶液:?。

参考答案:Fe;Fe-2e―=Fe2+;石墨或铜片;Cu2++2e―=Cu;氯化铜或硫酸铜溶液

本题解析:原电池中较活泼的金属是负极,失去电子,发生氧化反应。电子经导线传递到正极,所以溶液中的阳离子向正极移动,正极得到电子,发生还原反应。根据方程式可知,铁失去电子,发生氧化反应,所以铁是负极,电极反应式是Fe-2e―=Fe2+。铜离子得到电子,因此电解质溶液是含有铜离子的可溶性铜盐。而正极材料可以是石墨或金属性弱于铁的铜等,正极电极反应式是Cu2++2e―=Cu。
点评:该题是高考中的常见考点,侧重对学生基础知识的巩固和训练。有利于培养学生的逻辑推理能力和规范答题能力。明确原电池的工作原理、构成条件是答题的关键,注意相关知识的积累和总结。
本题难度:一般
2、选择题 下列每组的三种物质中,两边的固体均有导线连接,插入中间的液体中,其中能组成原电池的是( )
A.Zn|H2SO4(稀)|C
B.Cu|酒精|Ag
C.Zn|CCl4|Cu
D.Fe|H2SO4(稀)|Fe
参考答案:A、具备原电池的构成条件,所以能组成原电池,故A正确.
B、乙醇是非电解质,且不能自发的进行氧化还原反应,故B错误.
C、四氯化碳是非电解质,且不能自发的进行氧化还原反应,故C错误.
D、两电极活泼性相同,故D错误.
故选A.
本题解析:
本题难度:一般
3、选择题 一种新型的燃料电池,它以多孔镍板为电极插入KOH溶液中,然后分别向两极通入乙烷和氧气,其总反应为:2C2H6+7O2+8KOH=4K2CO3+10H2O,有关此电池的推断正确的是
[? ]
A.负极反应为14H2O+7O2+28e-=28OH-
B.放电过程中KOH的物质的量浓度不变
C.每消耗1molC2H6,则电路上转移的电子为14mol
D.放电一段时间后,负极周围的pH升高
参考答案:C
本题解析:
本题难度:一般
4、选择题 普通水泥在固化过程中自由水分子减少并产生Ca(OH)2,溶液呈碱性.根据这一物理化学特点,科学家发明了电动势法测水泥初凝时间.此方法的原理如图所示,反应的总方程式为:2Cu+Ag2O=CuO+2Ag,下列有关说法正确的是
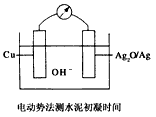
[? ]
A.普通水泥的主要成分是2CaO・SiO2,3CaO・SiO2和3CaO・Al2O3
B.测量原理示意图中,Ag2O为负极
C.正极的电极反应为:2Cu+2OH--2e-=Cu2O+H2O
D.电池工作时,OH-向正极移动
参考答案:A
本题解析:
本题难度:一般
5、选择题 下列说法正确的是( )
A.电化学腐蚀比化学腐蚀更普遍、腐蚀速度更快;但后者比前者的腐蚀危害更大
B.为防止电池中的重金属等污染土壤和水体,应积极开发废电池的综合利用技术
C.燃料电池是将燃料和氧化剂的化学能直接转换成电能的一次电池
D.钢铁发生吸氧腐蚀生成铁锈的过程中只发生了氧化还原反应
参考答案:A、电化学腐蚀过程中产生电流,电化学腐蚀比化学腐蚀普遍,腐蚀速度也快,导致电化学腐蚀比化学腐蚀危害大,故A错误.
B、电池中含有酸或碱和重金属,随便丢弃会对土壤和水体造成污染,所以应积极开发废电池的综合利用技术,故B正确.
C、燃料电池是将燃料和氧化剂的化学能直接转换成电能的原电池,不是一次电池,故C错误.
D、钢铁的吸氧腐蚀中,氢氧化铁脱去一部分水生成Fe2O3.xH2O的反应是非氧化还原反应,故D错误.
本题解析:
本题难度:简单