1������� ��14�֣�����ͼװ�ý���ʵ�飬���ش���������

��1���ж�װ�õ����ƣ�A��Ϊ_______ B��Ϊ______
��2��п��Ϊ______�����缫��ӦʽΪ______________
ͭ��Ϊ______�����缫��ӦʽΪ______________
ʯī��C1Ϊ_____�����缫��ӦʽΪ__________
ʯī��C2Ϊ_____��������������ʵ������Ϊ_____________
��3����C2������224mL���壨��״̬��ʱ��п�������仯�����ӻ���٣�____��_____g��CuSO4��Һ�������仯�ˣ����ӻ�����ˣ�_____��____g
�ο��𰸣���1��ԭ���?����
��2����? Zn - 2e- ="=" Zn2+
��? Cu2+ + 2e- ="=" Cu?����Cl- - 2e- ="=" Cl2��
��?��ɫ��Һ���ɫ
��3������? 0.65?����? 0.01
�����������
�����Ѷȣ���
2��ѡ���� ����������ڳ��ͷŵ�ʱ�����ķ�Ӧ��Fe+NiO2+2H2O
Fe��OH��2+Ni��OH��2�����жԸ������ƶϴ�����ǣ���������
�ٷŵ�ʱ��Fe���븺����Ӧ��NiO2����������Ӧ
�ڳ��ʱ�������ϵĵ缫��ӦʽΪ��Fe��OH��2+2e-�TFe+2OH-
�۷ŵ�ʱ���������Һ�е��������������ƶ�
�ܷŵ�ʱ�������ϵĵ缫��ӦʽΪ��Fe+2H2O-2e-�TFe��OH��2+2H+
�����صĵ缫�������ij�ּ��Ե������Һ�У�
A����
B���ۢ�
C����
D���٢ڢ�
�ο��𰸣���FeԪ�ػ��ϼ���0�۱�Ϊ+2�ۡ�NiԪ�ػ��ϼ���+4�۱�Ϊ+2�ۣ���Fe���븺����Ӧ��NiO2����������Ӧ������ȷ��
�ڳ��ʱ�������ϵõ��ӷ�����ԭ��Ӧ���缫��ӦʽΪFe��OH��2+2e-�TFe+2OH-������ȷ��
�۷ŵ�ʱ���������Һ�е��������������ƶ����������������ƶ�������ȷ��
�ܷŵ�ʱ��������ʧ���ӷ���������Ӧ���缫��ӦʽΪFe-2e-+2OH-=Fe��OH��2���ʴ���
���ɷ���ʽ��֪�˵��Ϊ���Ե�أ���Ӧ����ʽʱ���ܳ���H+��ֻ�ܽ��ڼ��Ե������Һ�У�����ȷ��
��ѡC��
���������
�����Ѷȣ���
3��ѡ���� �й���ͼװ���е�������ȷ���� (����)
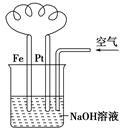
A�����ǵ��NaOH��Һ��װ��
B����Һ�з����˱仯��4Fe(OH)2��O2��2H2O=4Fe(OH)3
C��FeΪ�������缫��ӦΪ��Fe��2e����2OH��=Fe(OH)2
D��NaOH��Һ�ļ�������
�ο��𰸣�B
�������������װ�ÿ�֪����װ������ԭ��ء�����Pb���ã��������Ǹ�����Pb�����������ڵ����������������Һ��������������������ʴ����Ӧ�������������Ʋ�û�б����ģ����ܼ�ˮ���뷴Ӧ��������Һ�Ľ�������ǿ�ģ������ȷ�Ĵ�ѡB��
����������ԭ��غ͵��صĹؼ��ǿ�Ҳû����ӵ�Դ������ӵ�Դ�ľ��ǵ��أ���û����ӵ�Դ����ԭ��أ�Ȼ���ڷ����жϼ��ɡ������ʵ���ǿ��������������ʴ�ģ��ѶȲ���
�����Ѷȣ�һ��
4��ѡ���� ���������缫��������������Һ�У��������ֱ�ͨ�����������������ɼ���ȼ�ϵ�أ���֪ͨ������һ������缫��ӦΪCH4+10OH--8e-==== +7H2O;ͨ����������һ������缫��Ӧʽ��2O2+4H2O+8e-====8OH-������������ȷ���ǣ�?��
+7H2O;ͨ����������һ������缫��Ӧʽ��2O2+4H2O+8e-====8OH-������������ȷ���ǣ�?��
A��ͨ�����ĵ缫Ϊ����
B����������������Ӧ
C���õ��ʹ��һ��ʱ���Ӧ������������
D��ȼ�ϵ�ع���ʱ����Һ�е��������������ƶ�
�ο��𰸣�C
�������������ԭ���ԭ������������������Ӧ������������ԭ��Ӧ��ȷ��A����ȷ������CH4��������CO2��Ҫ����KOH����Ӧ���ϲ���KOH��
�����Ѷȣ�һ��
5������� ����ȼ�ϵ���Ƿ�����ɫ��ѧ��������ͷ���װ�á���ͼΪ���ʾ��ͼ���õ�ص缫�����һ��ϸС�IJ��ۣ��������������ǿ�������ȶ�����ش�
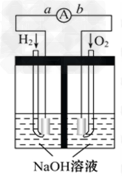
��1 ������ȼ�ϵ�ص�����ת����ʽ��Ҫ��______ ���ڵ����е�����������Ϊ______ ����a ��b ��ʾ����
��2 ��������ӦʽΪ__________________ ��
�ο��𰸣���1 ���ɻ�ѧ��ת��Ϊ���ܣ���a ��b
��2 ��2H2+4OH--4e- =4H2O�� H2+2OH--2e- =2H2O
���������
�����Ѷȣ�һ��