1、选择题 将0.1L含有0.02mol?CuSO4和0.01molNaCl的水溶液用惰性电极电解.电解一段时间后,一个电极上得到0.01mol?Cu,另一电极析出的气体( )
A.只有Cl2
B.只有O2
C.既有Cl2又有O2
D.只有H2
参考答案:溶液中含有n(Cu2+)=0.02mol,n(Cl-)=0.01mol;用惰性电极电解,电解一段时间后,一个电极上得到0.01mol Cu,是阴极反应,另一电极析出的气体为阳极反应;发生的电极反应为:根据得到铜物质的量计算电子转移,阳极电子转移守恒分析判断离子反应情况;
阳极电极反应:2Cl--2e-=Cl2↑;
?0.01mol 0.01mol
? 4OH--4e-=2H2O+O2↑
?0.01mol? 0.01mol
阴极电极反应:Cu2++2e-=Cu;
?0.02mol? 0.01mol
依据上述分析和计算得到,阳极反应生成的气体是氧气和氯气;
故选C.
本题解析:
本题难度:一般
2、选择题 下列说法中正确的是
A.在原电池中,物质在负极发生氧化反应
B.在原电池中,电子由正极流向负极
C.在电解池中,物质在阴极发生氧化反应
D.在电解池中,与电源正极相连的电极是阴极
参考答案:A
本题解析:在原电池中较活泼的金属作负极,失去电子,发生氧化反应。电子经导线传递到正极上,所以溶液中的阳离子向正极移动,阴离子向负极移动。正极得到电子,发生还原反应,所以选项A正确,其余选项都是错误的,答案选A。
考点:考查原电池的有关判断。
点评:原电池的正负极的判断(从原电池反应实质角度确定):
(1)由两极的相对活泼性确定:相对活泼性较强的金属为负极,一般地,负极材料与电解质溶液要能发生反应。
(2)由电极变化情况确定:某一电极若不断溶解或质量不断减少,该电极发生氧化反应,则此电极为负极;若某一电极上有气体产生、电极的质量不断增加或不变,该电极发生还原反应,则此电极为正极,燃料电池除外。
本题难度:一般
3、填空题 (8分).设计总反应为:2Fe3++Fe==3Fe2+原电池,在框内画出图示。并写出两极反应式。

正极:_______________________负极:_______________________
参考答案:(8分,图4分,电极反应各2分,设计合理就给分)
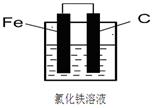
正极2Fe3++2e-=2Fe2+、负极Fe-2e-=Fe2+。
本题解析:根据离子方程式可知,铁离子得到电子,单质铁失去电子,所以原电池中负极材料是铁,正极材料是比铁不活泼的金属或石墨等,而电解质溶液中必须含有铁离子,例如氯化铁等,装置图如图所示(见答案)。其中电极反应式是正极2Fe3++2e-=2Fe2+、负极Fe-2e-=Fe2+。
点评:构成原电池的条件是活泼性不同的金属或金属和非金属,导线相连并插入到电解质溶液中,据此可以进行有关的判断。
本题难度:一般
4、选择题 某原电池装置如图所示。下列有关叙述中,正确的是
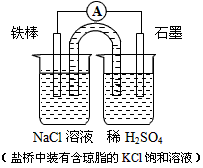
[? ]
A.Fe作正极,发生氧化反应
B.负极反应: 2H+ + 2e-=H2↑
C.工作一段时间后,两烧杯中溶液pH均不变
D.工作一段时间后,NaCl溶液中c(Cl-)增大
参考答案:D
本题解析:
本题难度:一般
5、选择题 A、B、C都是金属,把A浸入C的盐溶液中,A的表面有C析出,A与B和酸溶液组成原电池时,B为电池的负极。A、B、C金属的活动性顺序为 ( )
A.A>B>C B.A>C>B C.B>A>C D.B>C>A
参考答案:C
本题解析:把A浸入C的硝酸盐溶液中,A的表面有C析出;说明金属A可以把金属C从其盐中置换出来,所以活泼性A>C,A、B和稀硫酸组成原电池时,B为电池的负极,所以活泼性B>A,A、B、C三种金属的活动性顺序为B>A>C。
故选C。
考点:常见金属的活动性顺序及其应用 原电池和电解池的工作原理
点评:本题考查判断金属活泼性的方法,可以根据所学知识进行回答,难度不大。
本题难度:一般