1、填空题 原子序数由小到大排列的四种短周期元素X、Y、Z、W,四种元素的原子序数之和为32,在周期表中X是原子半径最小的元素,Y、Z左右相邻,Z、W位于同主族。
(1)W原子的核外电子排布式为_________。
(2)均由X、Y、Z三种元素组成的三种常见物质A、B、C分别属于酸、碱、盐,其化学式依次为_________、__________、_________,推测盐中阴离子的空间构型为__________,其中心原子杂化方式为__________。
(3)Z、W两种元素电负性的大小关系为____;Y、Z两种元素第一电离能的大小关系为____。
(4)CO的结构可表示为C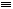 O,元素Y的单质Y2的结构也可表示为Y
O,元素Y的单质Y2的结构也可表示为Y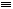 Y。右表是两者的键能数据(单位:kJ・mol-1):
Y。右表是两者的键能数据(单位:kJ・mol-1):
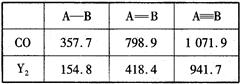
①结合数据说明CO比Y2活泼的原因:_____。
②意大利罗马大学Fulvio Cacace等人获得了极具研究意义的Y4分子,其结构如图所示,请结合上表数据分析,下列说法中,正确的是_____。
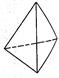
A.Y4为一种新型化合物? B.Y4与Y2互为同素异形体
C.Y4的沸点比P4(白磷)高? D.1 mol Y4气体转变为Y2将放出954.6kJ热量
参考答案:(1)1s22s22p63s23p4 (1分)
(2)HNO3、NH3・H2O 、NH4NO3 (3分)?平面三角形 (2分)? sp2 (1分)
(3)O>S或S<O (1分)? N>O 或O<N (1分)
(4)①断裂第一个π键消耗能量:CO 273kJ・mol-1< N2 523.3kJ・mol-1,CO中第一个π键更容易断裂,故CO比N2活泼 (3分)?② B、D (3分)
本题解析:原子序数由小到大排列的四种短周期元素X、Y、Z、W,四种元素的原子序数之和为32,在周期表中X是原子半径最小的元素,则X为氢元素;Y、Z左右相邻,Z、W位于同主族,原子序数Y<Z<W,则三者的相对位置为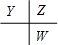 ,令Y的原子序数为a,则Z的原子序数为a+1,W的原子序数为a+9,所以a+a+1+a+9=32-1,解得a=7,故X为氢元素,Y为氮元素,Z为氧元素,W为硫元素。
,令Y的原子序数为a,则Z的原子序数为a+1,W的原子序数为a+9,所以a+a+1+a+9=32-1,解得a=7,故X为氢元素,Y为氮元素,Z为氧元素,W为硫元素。
(1)W为S元素,S原子的电子排布式为: 1s22s22p63s23p4 。
(2)H、N、O三种元素组成的三种常见物质,分别属于酸、碱、盐,为HNO3、NH3・H2O 、NH4NO3;NO3?中N原子作为中心原子提供5个电子,当第VIA族的元素O作为周围原子时,不提供电子,NO3?有一个负电荷,多1个电子,所以价电子一共6个,即3对。所以没有孤对电子,空间构型为平面三角形,中心原子杂化方式为sp2。
(3)O、S元素位于同主族,电负性O>S;第一电离能N>O。
(4)①CO断裂第一个π键消耗能量为1071.9kJ?mol?1-798.9kJ?mol?1=273kJ・mol-1, N2断裂第一个π键消耗能量为941.7 kJ?mol?1-418.4kJ?mol?1=523.3kJ・mol-1,CO中第一个π键更容易断裂,故CO比N2活泼。
②A、N4为单质,错误;B、N4与N2是N元素组成的结构和性质不同的单质,互为同素异形体,正确;C、N4与P4为结构相似的分子晶体,相对分子质量越大,范德华力越大,所以沸点N4<P4,错误;D、1 mol N4气体转变为N2放出的热量为:2mol×941.7kJ?mol?1-6mol×154.8kJ?mol?1=954.6kJ。
本题难度:一般
2、填空题 氮化钠(Na3N)是科学家制备的一种重要的化合物,它与水作用可产生NH3。请回答下列问题:
(1)Na3N的电子式是_______,该化合物由_______键形成的。
(2)Na3N与盐酸反应生成_____种盐,其电子式是______。
(3)Na3N与水的反应属于________反应。
(4)比较Na3N中两种粒子的半径:r(Na+)______r(N3-)(填“大于” “等于”或“小于”)。
参考答案:(1)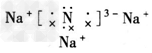 ;离子
;离子
(2)2;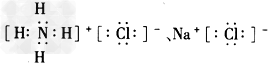
(3)复分解
(4)小于
本题解析:
本题难度:一般
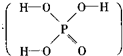
3、选择题 已知磷酸分子中的三个氢原子都可以跟重水分子(D2O)中的D原子发生氢交换.又知次磷酸(H3PO2)也可跟D2O进行氢交换,但次磷酸钠(NaH2PO2)却不能跟D2O发生氢交换.由此可推断出H3PO2的分子结构是( )
A.
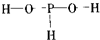
B.
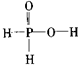
C.
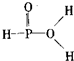
D.