1、选择题 在pH为4-5的环境中,Cu2+和Fe2+不水解,而Fe3+几乎完全水解。工业上制CuCl2是将浓盐酸用蒸汽加热到80℃左右。在漫漫加入粗氧化铜(含杂质FeO),充分搅拌使之溶解。欲除去所得CuCl2溶液中的杂质离子,下列方法中可行的是:?
A.加入HNO3将Fe2+氧化成Fe3+,再加水稀释至pH4-5
B.向溶液中通入Cl2,再加入CuO粉末调节至pH4-5
C.向溶液中通入Cl2,在通入NH3调节至pH4-
D.向溶液中通入H2O2, 再加入CuO粉末调节至pH4-5
参考答案:BD
本题解析:除杂质的同时不能引入新的杂质,也不能将所需要的物质给除去,才是成功的除杂;
A错,引入了硝酸根离子;B正确,C错,引入了铵根离子;D正确;
本题难度:一般
2、选择题 化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,正确的是(? )
A.用惰性电极电解饱和食盐水:2Cl-+ 2H+=H2↑+ Cl2↑
B.碱性氢氧燃料电池的正极反应式:O2+2H2O+4e-=4OH-
C.钢铁发生电化学腐蚀的正极反应式:Fe-2e-=Fe2+
D.碳酸钠溶液呈碱性:CO32-+2H2O=H2CO3+2OH-
参考答案:B
本题解析:电解饱和食盐水,参与的是H2O,生成碱,故A错误;碱性氢氧燃料电池正极O2得电子生成OH-,B正确;钢铁发生电化学腐蚀,铁做负极,C错误;碳酸钠溶液呈碱性是由于二元弱酸根CO32-发生了两步水解,D错误;故选B。
本题难度:一般
3、选择题 欲使0.1mol/L的NaHCO3溶液中c(H+)、c(CO32-)、c(HCO3-)都减少,其方法是
[? ]
A.通入二氧化碳气体
B.加入氢氧化钠固体
C.通入氯化氢气体
D.加入饱和石灰水
参考答案:D
本题解析:
本题难度:一般
4、选择题 Mg(OH)2在水中达到溶解平衡:Mg(OH)2(s) Mg2++2OH-,下列哪种情况可使Mg(OH)2(s)的量减少( )
Mg2++2OH-,下列哪种情况可使Mg(OH)2(s)的量减少( )
A.加入MgCl2溶液
B.加入少量NaOH
C.加入NH4NO3溶液
D.加入K2S溶液
参考答案:C
本题解析:A使[Mg2+]增大,B使[OH-]增大,均使平衡逆向移动,Mg(OH)2(s)的量增加,加入K2S溶液,S2-水解呈碱性,抑制Mg(OH)2固体溶解;加入NH4NO3,NH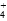 与OH-结合生成NH3・H2O,使[OH-]减小,平衡向右移动,促进Mg(OH)2(s)溶解。
与OH-结合生成NH3・H2O,使[OH-]减小,平衡向右移动,促进Mg(OH)2(s)溶解。
本题难度:一般
5、填空题 氯化铁水解的离子方程式为 ? ,向氯化铁溶液中加入碳酸钙粉末,发现碳酸钙逐渐溶解,并产生无色气体,其离子方程式为 ? 。同时有红褐色沉淀生成,其原因是 ? 。
参考答案:Fe3++3H2O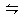 3H++Fe(OH)3;2H++CaCO3=Ca2++CO2↑+H2O;碳酸钙消耗了H+,使Fe3+水解平衡向右不断移动,造成Fe(OH)3不断增加,至出现红褐色沉淀。
3H++Fe(OH)3;2H++CaCO3=Ca2++CO2↑+H2O;碳酸钙消耗了H+,使Fe3+水解平衡向右不断移动,造成Fe(OH)3不断增加,至出现红褐色沉淀。
本题解析:氯化铁溶液中Fe3+水解的离子方程式为Fe3++3H2O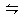 3H++Fe(OH)3;向氯化铁溶液中加入碳酸钙粉末,发现碳酸钙逐渐溶解,并产生无色气体,是由于Fe3+水解造成的酸性与碳酸钙反应的结果,即2H++CaCO3=Ca2++CO2↑+H2O;碳酸钙消耗了H+,使Fe3+水解平衡向右不断移动,造成Fe(OH)3不断增加,至出现红褐色沉淀。
3H++Fe(OH)3;向氯化铁溶液中加入碳酸钙粉末,发现碳酸钙逐渐溶解,并产生无色气体,是由于Fe3+水解造成的酸性与碳酸钙反应的结果,即2H++CaCO3=Ca2++CO2↑+H2O;碳酸钙消耗了H+,使Fe3+水解平衡向右不断移动,造成Fe(OH)3不断增加,至出现红褐色沉淀。
本题难度:一般