1������� ��12�֣�t��ʱ����3 mol A ��1 mol B���壬ͨ�����Ϊ2L���ܱ��������ݻ����䣩��������Ӧ��3A(g) + B��g��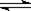 4 C��g�� 2minʱ��Ӧ�ﵽƽ��״̬���¶Ȳ��䣩�������C ��Ũ��Ϊ0.4 mol/L������д���пհף�
4 C��g�� 2minʱ��Ӧ�ﵽƽ��״̬���¶Ȳ��䣩�������C ��Ũ��Ϊ0.4 mol/L������д���пհף�
��1���ӷ�Ӧ��ʼ���ﵽƽ��״̬������C��ƽ����Ӧ����Ϊ_______________________��
��2���ﵽƽ��״̬ʱ��B ���ʵ�ת���ʦ�(B) =? _____________��
ƽ�ⳣ��K= _____________________(�������)��
��3����������ԭ�������ͨ�������������躤������A��B��C��Ӧ������ѧƽ��__________������ĸ��
A��������Ӧ�����ƶ�? B�����淴Ӧ�����ƶ�? C��ƽ�ⲻ�ƶ���
��4������ԭƽ�����ٳ���a mol C����t��ʱ�ﵽ��ƽ�⣬��ʱB�����ʵ���Ϊ��
n(B) =? ___________________ mol.
��5�����������Ӧ����ͬ�¶Ⱥ������н��У���ʹ��Ӧ�ﵽƽ��ʱC�����ʵ���������ԭƽ����ȣ���ʼ������������ʵ����ʵ���n(A)��n(B)��n(C)֮�������Ĺ�ϵΪ��
____________________________________��
�ο��𰸣���1��0.2mol/(L��min-1)����2��20% ��1/27=0.037?��3��C
��4��(0.8+0.2a)?��5��n(A)=3n(B)��n(C)>0
�����������1�� 2minʱC��Ũ��Ϊ0.4 mol/L����������C��ƽ����Ӧ����Ϊ0.2mol/(L��min-1)��

��3��ͨ������������������䣬��A��B��C��Ũ�Ȳ��䣬���ƽ�ⲻ�ƶ���
��4���ٳ���a mol C��������ֳ�����3/4amolA��1/4amolB����Ϊ��Ӧǰ�����������ʱA��B�����ʵ�����֮����Ȼ����3�U1����ƽ���������ƽ���Ч�����B��ת���ʻ���20�����ʴﵽ��ƽ�⣬B�����ʵ���Ϊ��1��0.25a��mol��80������0.8��0.2a��mol��
��5�����ݣ�4���ķ�����ֻ֪ҪA��B�����ʵ���֮������3�U1���ɡ�
�����Ѷȣ�һ��
2��ѡ���� ���Ѵ��ڻ�ѧƽ��״̬����ϵ�У���������������仯��һ���ܱ���ƽ���ƶ�����(? )
A����Ӧ������Ũ��
B����Ӧ���ת����
C�������淴Ӧ����
D����Ӧ������ѹǿ
�ο��𰸣�B
���������A �� �����Ӧǰ�����������ȣ�����ѹǿ������Ũ������ƽ�ⲻ�ƶ�
B �� ��Ӧ���ת���ʸı䣬ƽ��һ���ı�
C���� ���ʹ�ô����������淴Ӧ���ʶ�����ƽ�ⲻ�ƶ�
D ���������һƽ����ϵ�У�����ϡ�����壬ѹǿ����ƽ�ⲻ�ı䡣
�����Ѷȣ�һ��
3������� һ�������£���SO2��O2����һ�ܱ������У��������·�Ӧ��
2SO2��g��+O2��g�� 2SO3��g��������Ӧ���ȣ�
2SO3��g��������Ӧ���ȣ�
��Ӧ������SO2��O2��SO3���ʵ����仯��ͼ2-61��ʾ��

ͼ2-61
����������⣺
��1�������¶ȣ�SO2��ת����____________����ѧ��Ӧ�ٶ�____________�����������С�����䡱��
��2����Ӧ����ƽ��״̬��ʱ����____________��
��3����Ӧ������20 minʱ�����߷����仯��ԭ����________________________ �������ֱ����10 min��15 min�����߱仯��ԭ�������____________����д��ţ���
a.���˴���
b.���������
c.�����¶�
d.����SO3�����ʵ���
�ο��𰸣���1�������С��2��15��20 min,25��30 min(3)������O2����? ab
�����������1�����£�ƽ��������Ӧ�����ƶ���SO2��ת��������ѧ��Ӧ���ʽ��͡�
��2����Ӧ����15 minʱ��SO2��O2��SO3�����ʵ������������仯��˵����Ӧ�ﵽ��ƽ��״̬��
��3����Ӧ������20 min��O2�����ʵ�������ͻ�䣬˵����ʱ������O2������
�����Ѷȣ�һ��
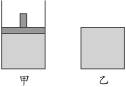
4�������� ����ͬ���ʵ�����SO3������������������У���֪�������л������������ƶ�������������̶�������ͬ���¶ȡ�ѹǿ�¿�ʼ������Ӧ��2SO3(g) ?2SO2(g)+O2(g)���ڷ�Ӧ������ά����ϵ�¶Ȳ��䡣
?2SO2(g)+O2(g)���ڷ�Ӧ������ά����ϵ�¶Ȳ��䡣
��1����ﵽƽ��״̬ʱSO3�����ת���ʵĴ�С��ϵ��
 ͼ2-2
ͼ2-2
��2���ﵽƽ��״̬ʱ�ֱ����һ������Ar����ƽ���Ƿ���ƶ����������ƶ���
�ο��𰸣���1����������SO3��ת���ʱ���������SO3��ת����Ҫ��
��2��������ƽ��������Ӧ�����ƶ���SO3��ת��������������ƽ�ⲻ�ƶ�
�����������ʼʱ����������SO3�����ʵ�����������¶ȶ�����ȵģ������ڷ�Ӧ������ά���¶Ȳ��䣬�������������¶�ʼ������ͬ�ģ����ڷ�Ӧ��һ�����������Ŀ����ķ�Ӧ�����Զ�����������˵�����ŷ�Ӧ�IJ��Ͻ�����ѹǿ���������������������������Ŀ�����࣬�������������ƶ���������������������������൱����A�����Ļ����Ͻ��м�ѹ�������ڿ��淴Ӧ2SO3(g) ?2SO2(g)+O2(g)����ѹ��ʹ��ƽ�����淴Ӧ�����ƶ���������ʹת���ʼ�С�����Դﵽƽ��״̬ʱ��������SO3��ת���ʱ���������SO3��ת����Ҫ��
?2SO2(g)+O2(g)����ѹ��ʹ��ƽ�����淴Ӧ�����ƶ���������ʹת���ʼ�С�����Դﵽƽ��״̬ʱ��������SO3��ת���ʱ���������SO3��ת����Ҫ��
�����������ж��ﵽƽ��״̬���ٷֱ����һ������Ar�����������������û�иı䣬��Ӧ��ϵ�и������ʵ�Ũ�Ȳ�û�б仯�������淴Ӧ������Ȼ��ȣ�������ƽ�ⲻ���ƶ������������ڻ������ƶ��ᵼ����������������ʵ�Ũ��ͬ�ȱ�����С�����ֱ�ӽ�����������һ����������ʱ������൱��ѹǿ��С����ƽ��������Ӧ�����������Ŀ���ࣩ�����ƶ���SO3��ת����Ҫ����
�����Ѷȣ���
5��ѡ���� һ���¶��£�ij�ܱ������д��ڿ��淴Ӧ��X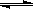 Y+Z,�仯ѧ��Ӧ������ʱ��仯��ͼ����ͼ��ʾ������t1ʱ�̴ﵽƽ�⣬t2ʱ����С���������t3ʱ�����´ﵽƽ�⣬�����й�˵������ȷ����(? )
Y+Z,�仯ѧ��Ӧ������ʱ��仯��ͼ����ͼ��ʾ������t1ʱ�̴ﵽƽ�⣬t2ʱ����С���������t3ʱ�����´ﵽƽ�⣬�����й�˵������ȷ����(? )

A��X�ڸ�������һ����Ϊ����
B��Y��Z�ڸ�������������һ��Ϊ����
C��t1ʱ�̴ﵽƽ��ʱ��t3ʱ��ƽ��ʱ����̬���ʵ�Ũ����ͬ
D����t1��t3��ƽ�Ⲣδ�����ƶ���
�ο��𰸣�D
�������������ͼ���֪������ѹǿ������Ӧ���ʲ��䣬�淴Ӧ����������˵����Ӧ����û�����壬�������к������塣�������ε�ƽ���з�Ӧ��������ͬ�ģ�������̬���ʵ�Ũ����ͬ������ͼ���֪��ƽ�����淴Ӧ�����ƶ�������ѡ��D�Ǵ���ģ������ȷ����ѡD��
�����Ѷȣ�һ��