1、实验题 (11分).请利用下列装置及试剂组装一套装置。其流程是,先制取纯净干燥的Cl2(不收集),后试验干燥的Cl2和潮湿的Cl2有无漂白性。试回答:
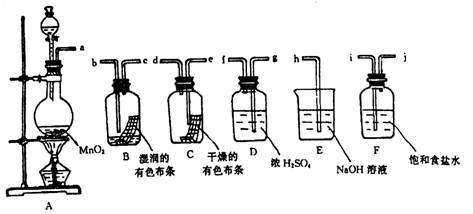

(1)按气体从左向右流向将各装置依次连接起来(填接口标号): a 接_______,______
接______ ,______ 接______ ,______ 接______ ,______ 接h。
(2)烧瓶中发生反应的化学方程式是________________________________________ 。
(3)D装置的作用是____________________ ,E装置的作用是____________________ ,
F装置的作用 是 ________________________。
是 ________________________。
(4)C瓶中的现象是______________________ ,B瓶中的现象是___________________ 。以上事实说明起漂白作用的物质是___________________ 。
2、实验题 下图是实验室制备氯气并进行一系列相关实验的装置(夹持设备已略)。
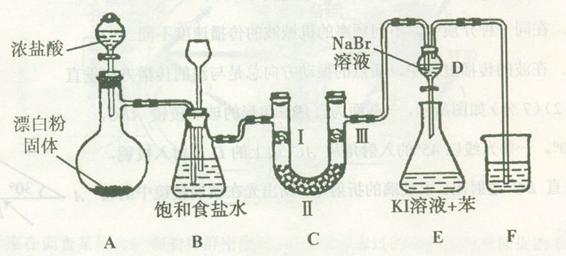
(1)装置A是氯气的发生装置,请写出相应反应的化学方程式:??。
(2)装置B中饱和食盐水的作用是?;同时装置B也是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象:?。
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中I、II、III处依次放入物质的组合应是? (填字母编号)。
编号
| I
| II
| III
|
a
| 干燥的有色布条
| 碱石灰
| 湿润的有色布条
|
b
| 干燥的有色布条
| 无水硫酸铜
| 湿润的有色布条
|
c
| 湿润的有色布条
| 浓硫酸
| 干燥的有色布条
|
d
| 湿润的有色布条
| 无水氯化钙
| 干燥的有色布条
|
?
(4)设计装置D、E的目的是比较氯、溴、碘单质的氧化性。反应一段时间后,打开活塞,将装置D中少量溶液加入装置E中,振荡,观察到的现象是 ?,该现象?(填“能”或“不能”)说明溴单质的氧化性强于碘,原因是?。
(5)装置F的作用是?,其烧杯中的溶液不能选用下列中的 ?(填字母编号)。
a.饱和NaOH溶液? b.饱和Ca(OH)2溶液
c.饱和Na2SO3溶液? d.饱和Na2CO3溶液
3、选择题 下列说法正确的是( )
A.新制氯水是混合物,久置氯水是纯净物
B.氯气在氢气中燃烧生成的气体溶于水中形成盐酸
C.次氯酸钙比次氯酸不稳定
D.漂白粉的有效成分是Ca(ClO)2和CaCl2
4、选择题 下列有关化学反应过程或实验现象的叙述中,正确的是(?)
A.氨气的水溶液可以导电,说明氨气是电解质
B.漂白粉和明矾都常用于自来水的处理,二者的作用原理是相同的
C.在滴有酚酞的Na2CO3溶液中慢慢滴入BaCl2溶液,溶液的红色逐渐褪去
D.氯气可以使湿润的有色布条褪色,说明氯气具有漂白作用
5、实验题 实验室制备气体时,可根据反应物的状态、反应条件和生成气体的性质来选择气体的发生装置。
(1)实验室用氯酸钾和二氧化锰制氧气时,可选用的发生装置是?(写编号);
(2)实验室用食盐固体和浓硫酸制氯化氢气体时,可选用的发生装置是?(写编号),写出微热时的反应方程式??;
(3)高锰酸钾和二氧化锰都是强氧化剂,均可将浓盐酸氧化为氯气。
(a) 用浓盐酸和高锰酸钾制氯气的反应方程式如下:
2KMnO4 + 16HCl 2KCl + 2MnCl2 + 5Cl2 ↑?+ 8H2O
2KCl + 2MnCl2 + 5Cl2 ↑?+ 8H2O
①用“单线桥”在上述方程式上标出电子转移的方向和数目。
②反应中?元素被氧化,?是氧化剂。当有1mol电子转移时,可生成气体?升(标准状态下)。
(b) 用浓盐酸和二氧化锰制氯气的实验装置如图所示:
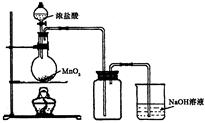
写出圆底烧瓶中发生反应的化学方程式_??
②实验结束清洗仪器时,为了减少烧瓶中残留氯气对环境的污染,可以向烧瓶中加入的溶液是________,有关的化学方程式_________________________.