1、实验题 (11分).请利用下列装置及试剂组装一套装置。其流程是,先制取纯净干燥的Cl2(不收集),后试验干燥的Cl2和潮湿的Cl2有无漂白性。试回答:
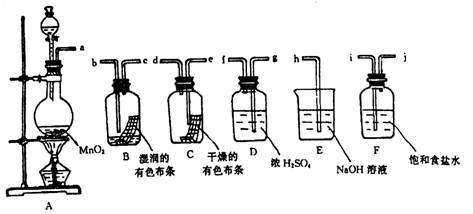

(1)按气体从左向右流向将各装置依次连接起来(填接口标号): a 接_______,______
接______ ,_ _____ 接______ ,______ 接______ ,______ 接h。
(2)烧瓶中发生反应的化学方程式是________________________________________ 。
(3)D装置的作用是____________________ ,E装置的作用是____________________ ,
F装置的作用 是 ________________________。
是 ________________________。
(4)C瓶中的现象是______________________ ,B瓶中的现象是___________________ 。以上事实说明起漂白作用的物质是___________________ 。
参考答案:(1)i;j;g;f;e;d;b;c;
(2)MnO2+4HCl(浓)  MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
(3)干燥氯气?吸收多余的氯气?除去HCl气体
(4)有色布条不褪色?有色布条褪色?次氯酸(HClO)
本题解析:略
本题难度:一般
2、实验题 下图是实验室制备氯气并进行一系列相关实验的装置(夹持设备已略)。
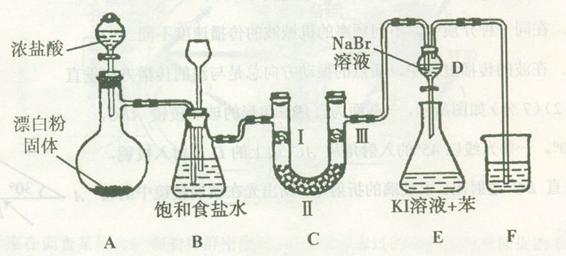
(1)装置A是氯气的发生装置,请写出相应反应的化学方程式:??。
(2)装置B中饱和食盐水的作用是?;同时装置B也是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象:?。
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中I、II、III处依次放入物质的组合应是? (填字母编号)。
编号
| I
| II
| III
|
a
| 干燥的有色布条
| 碱石灰
| 湿润的有色布条
|
b
| 干燥的有色布条
| 无水硫酸铜
| 湿润的有色布条
|
c
| 湿润的有色布条
| 浓硫酸
| 干燥的有色布条
|
d
| 湿润的有色布条
| 无水氯化钙
| 干燥的有色布条
|
?
(4)设计装置D、E的目的是比较氯、溴、碘单质的氧化性。反应一段时间后,打开活塞,将装置D中少量溶液加入装置E中,振荡,观察到的现象是 ?,该现象?(填“能”或“不能”)说明溴单质的氧化性强于碘,原因是?。
(5)装置F的作用是?,其烧杯中的溶液不能选用下列中的 ?(填字母编号)。
a.饱和NaOH溶液? b.饱和Ca(OH)2溶液
c.饱和Na2SO3溶液? d.饱和Na2CO3溶液
参考答案:(1)Ca(ClO) 2+4HCl(浓)=CaCl2+2Cl2↑+2H2O
(2)除去Cl2中的HCl ? B中长颈漏斗中液面上升,形成水柱
(3)d
(4)E中溶液分为两层,上层(苯层)为紫红色?不能 ?过量的Cl2也可将I-氧化为I2
(5)吸收余氯,防止污染大气? b
本题解析:(1)漂白粉中的Ca(ClO)2与浓盐酸反应生成Cl2,化学方程式为:Ca(ClO) 2+4HCl(浓)==CaCl2+2Cl2↑+2H2O
(2)用浓盐酸制取的Cl2中含有HCl,所以装置B中饱和食盐水的作用是除去Cl2中的HCl;如果C中发生堵塞,B中压强增大,则B中长颈漏斗中液面上升,形成水柱。
(3)为了验证氯气是否具有漂白性,I中加入湿润的有色布条,II为U型管,可加入固体干燥剂,得到干燥的Cl2,III中加入干燥的有色布条,即可证明Cl2是否具有漂白性,故d项正确。
(4)装置D中试剂为溴水,加入到E中,Br2与I?反应生成I2,所以实验现象为:E中溶液分为两层,上层(苯层)为紫红色;Cl2通入D与NaBr反应生成Br2,可能会有Cl2剩余,所以把D中溶液加入到E中,也有可能是Cl2将I?氧化为I2,因此不能说明溴单质的氧化性强于碘。
(5)Cl2有毒,需要进行尾气处理,所以装置F的作用是吸收余氯,防止污染大气;A、Cl2能与NaOH溶液反应,被吸收,正确;b、因为Ca(OH)2微溶于水,饱和Ca(OH)2溶液浓度小,不能充分吸收Cl2,错误;C、Cl2具有较强氧化性,能氧化Na2SO3,被吸收,正确;D、Cl2能与Na2CO3溶液反应,生成NaCl、NaClO、NaHCO3,被吸收,正确。
本题难度:一般
3、选择题 下列说法正确的是( )
A.新制氯水是混合物,久置氯水是纯净物
B.氯气在氢气中燃烧生成的气体溶于水中形成盐酸
C.次氯酸钙比次氯酸不稳定
D.漂白粉的有效成分是Ca(ClO)2和CaCl2
参考答案:A、新制氯水含有氯气、氯离子、氢离子、氢氧根离子、次氯酸根离子,次氯酸分子、水分子7种微粒,久置氯水即为盐酸溶液,含有氯离子、氢离子、氢氧根离子,成分有区别,故A错误;
B、氯气在氢气中燃烧生成氯化氢气体,HCl极易溶于水形成盐酸,故B正确;
C、次氯酸受热易分解,次氯酸钙易和空气成分水以及二氧化碳反应而变质,二者都不稳定,故C错误;
D、漂白粉的有效成分是Ca(ClO)2,成分是Ca(ClO)2和CaCl2的混合物,故D错误.
故选B.
本题解析:
本题难度:一般
4、选择题 下列有关化学反应过程或实验现象的叙述中,正确的是(?)
A.氨气的水溶液可以导电,说明氨气是电解质
B.漂白粉和明矾都常用于自来水的处理,二者的作用原理是相同的
C.在滴有酚酞的Na2CO3溶液中慢慢滴入BaCl2溶液,溶液的红色逐渐褪去
D.氯气可以使湿润的有色布条褪色,说明氯气具有漂白作用
参考答案:C
本题解析:A错,氨气属于非电解质;B错,漂白粉净水原理为强氧化性,明矾净水为生成了氢氧化铝胶体,胶体的吸附作用净水;C正确;D错,氯气本身无漂白性,只有与水反应生成了HCLO,HCLO具有漂白性;
本题难度:一般
5、实验题 实验室制备气体时,可根据反应物的状态、反应条件和生成气体的性质来选择气体的发生装置。
(1)实验室用氯酸钾和二氧化锰制氧气时,可选用的发生装置是?(写编号);
(2)实验室用食盐固体和浓硫酸制氯化氢气体时,可选用的发生装置是?(写编号),写出微热时的反应方程式??;
(3)高锰酸钾和二氧化锰都是强氧化剂,均可将浓盐酸氧化为氯气。
(a) 用浓盐酸和高锰酸钾制氯气的反应方程式如下:
2KMnO4 + 16HCl 2KCl + 2MnCl2 + 5Cl2 ↑?+ 8H2O
2KCl + 2MnCl2 + 5Cl2 ↑?+ 8H2O
①用“单线桥”在上述方程式上标出电子转移的方向和数目。
②反应中?元素被氧化,?是氧化剂。当有1mol电子转移时,可生成气体?升(标准状态下)。
(b) 用浓盐酸和二氧化锰制氯气的实验装置如图所示:
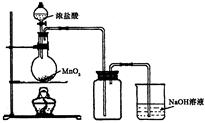
写出圆底烧瓶中发生反应的化学方程式_??
②实验结束清洗仪器时,为了减少烧瓶中残留氯气对环境的污染,可以向烧瓶中加入的溶液是________,有关的化学方程式_________________________.
参考答案:(1) A?(2) C ; NaCl + H2SO4 NaHSO4? +? HCl↑;(3)(a)?
NaHSO4? +? HCl↑;(3)(a)?
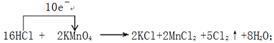 ? Cl元素;KMnO4;11.2
? Cl元素;KMnO4;11.2
(b) ①? MnO2 + 4HCl(浓)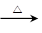 2MnCl2 + Cl2↑ + 2 H2O?
2MnCl2 + Cl2↑ + 2 H2O?
②NaOH;? Cl2 ?+ 2 OH- Cl-?+?ClO- +? H2O
Cl-?+?ClO- +? H2O
本题解析:根据装置图可知,A适用于固体和固体加热制备气体的。B装置适用于液体和固体或液体和液体之间不需要加热制备气体的。C装置适用于液体和固体或液体和液体之间需要加热制备气体的。
(1)实验室用氯酸钾和二氧化锰制氧气时,属于固体和固体之间加热制备气体的,所以可选用的发生装置是A。
(2)实验室用食盐固体和浓硫酸制氯化氢气体时,属于液体和固体之间加热制备气体的,所以可选用的发生装置是C,反应的化学方程式是NaCl + H2SO4 NaHSO4 + HCl↑。
NaHSO4 + HCl↑。
(3)(a)根据方程式可知,Mn元素的化合价从+7价降低到+2价,得到5个电子,则高锰酸钾是氧化剂。氯化氢中氯元素的化合价从-1价升高到0价,失去1个电子,则氯化氢是还原剂,氯元素被氧化。所以根据电子得失守恒可知,其表示方法是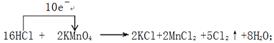
当有1mol电子转移时,可生成0.5mol氯气,在标准状况下的体积是22.4L/mol×0.5mol=11.2L。
(b)① 在加热的条件下,二氧化锰能把浓盐酸氧化生成氯气,则反应的化学方程式是 MnO2 + 4HCl(浓)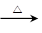 2MnCl2 + Cl2↑ + 2 H2O。
2MnCl2 + Cl2↑ + 2 H2O。
②氯气有毒,需要尾气处理,试剂选用氢氧化钠溶液,反应的离子方程式是 Cl2 + 2 OH- Cl-?+?ClO- +? H2O。
Cl-?+?ClO- +? H2O。
点评:该题是高考中的常见题型,属于中等难度实验题的考查,该题紧扣教材基础知识,有利于调动学生的学习兴趣,激发学生的学习积极性,有利于培养学生规范严谨的实验设计能力,提升学生的学科素养。该类试题主要是以常见仪器的选用、实验基本操作为中心,通过是什么、为什么和怎样做重点考查实验基本操作的规范性和准确性及灵活运用知识解决实际问题的能力。
本题难度:一般