1、选择题 下列叙述中正确的是()
A.化反应一定有物质变化,不一定有能量变化
B.化合反应一定是放热反应
C.放热反应不需要加热就一定能发生
D.吸热反应不加热也可能发生
参考答案:D
本题解析:略
本题难度:简单
2、填空题 (6分)氢气燃烧生成液态水的热化学方程式是:2H2(g)+O2(g) ===2H2O(l);ΔH=-572kJ/mol?请回答下列问题:
(1)生成物能量总和 (填“大于”、“小于”或“等于”)反应物能量总和。
(2)若2 mol氢气完全燃烧生成水蒸气,则放出的热量?572 kJ (填“>”、“<”或“=”)。
(3)美国阿波罗宇宙飞船上使用了一种新型装置,其构造如图所示,a、b两个电极均由多孔的碳块组成。它是将 ? 能转化为 能的装置。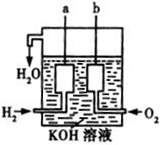
参考答案:小于、<、化学,电
本题解析:化学反应中必然伴随着能量变化。如果反应物的总能量高于生成物的总能量,就是放热反应,反之是吸热反应。由于水蒸气的能量高于液态水的能量,所以氢气燃烧生成液态水放出的能量要高于生成气态水放出的能量;原电池是把化学能转化为电能的一种装置。
本题难度:一般
3、选择题 科学家已获得了极具理论研究意义的N4分子,其结构为正四面体(如图所示),与白磷分子相似。已知断裂1 mol N―N键吸收193 kJ热量,断裂1 mol N≡N键吸收941 kJ热量,则()
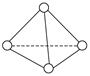
A.N4的熔点比P4高
B.1 mol N4气体转化为N2时要吸收724 kJ能量
C.N4是N2的同系物
D.1 mol N4气体转化为N2时要放出724 kJ能量
参考答案:D
本题解析:N4与白磷(P4)结构相似,均为分子晶体,由于N4相对分子质量小于P4,故其分子间作用力弱于P4,其熔点低于P4,A错;N4与N2互为同素异形体,而不是同系物,则C错;从结构图中可看出,一个N4分子中含有6个N―N键,根据N4(g)===2N2(g) ΔH,有ΔH=6×193 kJ・mol-1-2×941 kJ・mol-1=-724 kJ・mol-1,故B项错误,D项正确,答案选B。
点评:该题是高考中的常见题型,属于中等难度的试题。试题综合性强,侧重对学生基础知识的巩固和训练,主要是考查学生对晶体类型以及反应热计算的熟悉了解程度,有利于调动学生的逻辑推理能力和发散思维能力,提高学生灵活运用基础知识解决实际问题的能力。该题的关键是明确物质熔点高低额判断依据和反应热的计算依据,然后结合题意灵活运用即可。
本题难度:简单
4、填空题 利用光能和光催化剂,可将 CO2和 H2O(g)转化为 CH4和 O2。紫外光照射时,在不同催化剂(Ⅰ,Ⅱ,Ⅲ)作用下,CH4产量随光照时间的变化如图所示。

(1)在0~30 小时内,CH4的平均生成速率 vⅠ、vⅡ和vⅢ从大到小的顺序为________;反应开始后的 12 小时内,在第________种催化剂作用下,收集的 CH4最多。
(2)将所得 CH4与 H2O(g)通入聚焦太阳能反应器,发生反应:CH4(g)+H2O(g)  CO(g)+3H2(g)。该反应ΔH=+206 kJ・mol-1。
CO(g)+3H2(g)。该反应ΔH=+206 kJ・mol-1。
①画出反应过程中体系能量变化图(进行必要标注)。
②将等物质的量的CH4和 H2O(g)充入 1 L 恒容密闭反应器中,某温度下反应达到平衡,平衡常数 K = 27,此时测得 CO 的物质的量为 0.10 mol,求CH4的平衡转化率(计算结果保留两位有效数字)。
(3)已知:CH4(g)+2O2(g)=CO2(g)+2H2O(g)ΔH=-802 kJ・mol-1。
写出由 CO2生成 CO 的热化学方程式____________________________________
参考答案:(1)vⅢ>vⅡ>vⅠ Ⅱ
(2)①
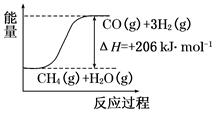
②91%
(3)CO2(g)+3H2O(g)=CO(g)+3H2(g)+2O2(g)
ΔH=+1008 kJ・ mol-1
本题解析:本题考查化学反应速率和化学平衡,意在考查考生的识图能力、三段式解决化学平衡问题能力和盖斯定律的使用。(1)0~30小时内,CH4的平均速率=,由图可知,30小时内CH4的产量Ⅲ>Ⅱ>Ⅰ,即CH4的平均生成速率的关系为vⅢ>vⅡ>vⅠ;前12小时内在第Ⅱ种催化剂作用下,收集的CH4最多。
(2)①该反应中,CH4的用量越多,吸收的热量越多,二者成正比例关系,标注反应热注意二者的对应关系。
②假设CH4和H2O的起始量均为x mol,结合平衡时n(CO)=0.10 mol,有:
CH4(g)+H2O(g)=CO(g)+3H2(g)
起始浓度(mol・L-1) x x 0 0
变化量(mol・L-1)?0.10 ?0.10 ?0.10? 0.30
平衡浓度(mol・L-1)? x-0.10?x-0.10?0.10? 0.30
结合K===27,
解得x=0.11 mol・L-1,
CH4的转化率=×100%=91%。
(3)结合题目所给的两个热化学反应方程式,根据盖斯定律,将两方程式作差即可。
本题难度:一般
5、实验题
Ⅰ.已知测定中和热的实验步骤如下:①量取50mL 0.25 mol/L硫酸倒入小烧杯中,测量温度?②量取50mL 0.55mol/L NaOH溶液,测量温度;?③将NaOH溶液倒入小烧杯中,混合均匀后测量混合液温度。请回答:
(1)NaOH溶液稍过量的原因?。
(2)加入NaOH溶液的正确操作是? (填字母)。
A.沿玻璃棒缓慢加入? B.一次迅速加入? C.分三次加入
(3)使硫酸与NaOH溶液混合均匀的正确操作是?。
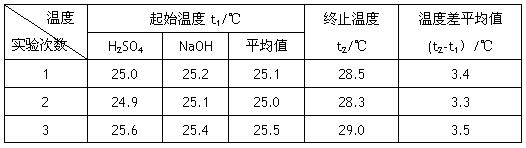
(4)设溶液的密度均为1g・cm-3,中和后溶液的比热容c="4.18" J・(g・℃)-1,请根据实验数据求出中和热为 ? 写出该反应的热化学方程式_________?
(5)若将含0.5 mol H2SO4的浓硫酸与含1 mol NaOH的溶液混合,放出的热量?(填“小于”、“等于”或“大于”)57.3 kJ,原因是 ? ?
Ⅱ.某烧碱样品含有少量不与酸作用的杂质,为了测定其纯度,进行以下操作:
A.在250 mL的容量瓶中定容配成250 mL烧碱溶液
B.用碱式滴定管量取25.00 mL烧碱溶液于锥形瓶中,并滴入几滴酚酞作指示剂
C.在天平上准确称取烧碱样品W g,在烧杯中用蒸馏水溶解
D.将物质的量浓度为M的标准硫酸溶液装入润洗好的酸式滴定管中,调节液面使开始读数为V1 mL
E.在锥形瓶下垫一张白纸,滴定至溶液恰好由红色变为无色时,记下读数为V2 mL
试填空:
(1)正确操作步骤的顺序是??(用字母表示)。
(2)观察滴定管液面的高度时应注意?
?
(3)E步骤的操作中锥形瓶下垫一张白纸的作用是??。
(4)某学生实验时把锥形瓶用烧碱样品溶液洗涤,使测定的浓度_________(填“偏高”“偏低”或“无影响”),原因是??
(5)该烧碱样品纯度的计算式为_________________________。
参考答案:Ⅰ、(1)确保硫酸被完全中和 (2)B? (3)用环形玻璃棒轻轻搅动
(4)56.85 kJ・mol-1 ?, H2SO4(aq)+2NaOH(aq)=Na2SO4(aq)+2H2O?ΔH=-113.7kJ・mol-1
(5)大于?浓硫酸溶于水放出热量
Ⅱ.答案:(1)CABDE
(2)滴定管要直立,装液后需等1~2 min后才能观察液面高度;读数时视线与液体的凹液面及刻度线在同一水平面上,读数应准确至0.01 mL
(3)使滴定终点颜色变化更明显,便于分辨? (4)偏高
因碱液样品沾在锥形瓶内壁使烧碱的物质的量增加,耗用标准酸的体积偏大,故烧碱浓度偏高
(5)0.8(V2-V1)M/W×100%
本题解析:略
本题难度:简单