1、填空题 已知在催化剂存在条件下,能发生如下反应:
CO + H2O(g)  H2 + CO2 + Q
H2 + CO2 + Q
(1)在5 L盛有固体催化剂(其体积可忽略不计)的密闭容器中,通入反应物,10 s后,生成了氢气0.2 g,则此10 s内CO的平均反应速率为v(CO) = ____?_0.002 mol/Ls______。
(2)在该密闭容器中,下列叙述可以说明反应已经达到平衡状态的是__?BC___
A.若容器体积不变,在一定温度下压强达到恒定
B.CO2的生成速率与H2O蒸气的生成速率之比为1 : 1
C.CO、H2O、H2、CO在容器中的物质的量浓度保持不变
D.反应体系中混合物的平均摩尔质量保持不变
(3)在上述反应达平衡状态后,分别改变条件,请完成下列两张图:
A.在第20 s时将容器体积缩小至? B.在第20 s时,向容器中注入少量的
原来的一半后压强变化图? CO气体后正逆反应速率变化图
参考答案:(1)v(CO) = __2×10-3mol/Ls___。(2)__BCBC___
(3)A.在第20 s时将容器体积缩小至? B.在第20 s时,向容器中注入少量的
原来的一半后压强变化图? CO气体后正逆反应速率变化图

本题解析:略
本题难度:简单
2、选择题 对于已达平衡状态的反应:X(g)+3Y(g)? 2Z(g)(正反应为放热反应),为了使平衡向生成Z的方向移动,应选择下列的适宜条件是(?)
2Z(g)(正反应为放热反应),为了使平衡向生成Z的方向移动,应选择下列的适宜条件是(?)
①高温?②低温?③高压?④低压?⑤加催化剂?⑥除去Z
A.①④⑥
B.②③⑤
C.①③⑥
D.②③⑥
参考答案:D
本题解析:生成Z的方向就是正反应方向,根据勒夏特列原理,可采取加压,降温,降低Z浓度的方法促使其向正反应方向移动。答案应选D。
本题难度:简单
3、填空题 (2分)在密闭容器中进行下列反应,CO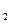 (g)+C(s)
(g)+C(s) 2CO(g)? △H>0,当反应达平衡后,改变下列条件,则指定物质的平衡如何变化:
2CO(g)? △H>0,当反应达平衡后,改变下列条件,则指定物质的平衡如何变化:
(1)增加C的用量,平衡___________移动(选填正向、逆向、不);
(2)保持温度不变,减小容器体积,平衡___________移动(选填正向、逆向、不)。
参考答案:

本题解析:略
本题难度:一般
4、选择题 可以说明反应2HI(g) H?2(g)+I2(g)已达到平衡的是(? )
H?2(g)+I2(g)已达到平衡的是(? )
①单位时间内生成n mol H2的同时生成n mol HI
②一个H-H键断裂的同时有两个H-I键断裂
③百分组成ω(HI)=ω(I2)
④反应速率υ(H2)=υ(I2)=1/2υ(HI)时
⑤ c(HI):c(H2):c(I2)=2:1:1时
⑥温度和体积一定时,容器内压强不再变化
⑦温度和体积一定时,某一生成物浓度不再变化
⑧条件一定,混合气体的平均相对分子质量不再变化
⑨温度和体积一定时,混合气体的颜色不再变化
⑩温度和压强一定时,混合气体的密度不再变化
A.②③⑤?B.①④⑦?C.②⑦⑨?D⑧⑨⑩
参考答案:C
本题解析:判断某可逆是否达到平衡的本质:1、平衡时体系中各组分的浓度保持不变;2、正、逆反应速率相等且不等于0;①错,每时每刻均这样反应;②正确;③错,平衡时不是各组分的百分含量相等而是各组分的百分含量保持不变;④错,每时每刻都是υ(H2)=υ(I2)=1/2υ(HI);⑤错,平衡时各组分的浓度可能相等也可能不相等;⑥错,该反应为等体积反应,无论是否平衡容器内压强均不变;⑦正确;⑧错,反应为等体积反应且状态都是气体,条件一定,混合气体的平均相对分子质量始终不变;⑨正确;⑩错,由于反应为等体积反应,密度为常数;
本题难度:一般
5、选择题 某温度下,反应2NO2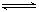 N2O4;△H<O,在密闭容器中达到平衡。平衡时改变外界条件,使反应再次平衡,新平衡时,c(NO2)/c(N2O4)与原平衡相比变大了,则改变条件的可能有
N2O4;△H<O,在密闭容器中达到平衡。平衡时改变外界条件,使反应再次平衡,新平衡时,c(NO2)/c(N2O4)与原平衡相比变大了,则改变条件的可能有
A.保持容器容积和温度不变,向容器内补充了NO2
B.保持容器压强和温度不变,向容器内补充了N2O4
C.保持容器容积和温度不变,向容器内补充了N2
D.保持容器的容积不变,升高了温度
参考答案:D
本题解析:定温定容时,向容器中充NO2,平衡向右移动,c(NO2)/c(N2O4)减小;定温定压时,向容器中充入N2O4,平衡不移动,c(NO2)/c(N2O4)不变;定温定容时向容器中充N2,平衡不移动,c(NO2)/c(N2O4)不变;保持容器体积不变,升高温度,平衡向左移动,c(NO2)/c(N2O4)增大。
点评:分清定温定容还是定温定压。
本题难度:一般