1、实验题 (12分)为研究铁质材料与热浓硫酸的反应,某小组进行了以下探究活动:
【探究一】称取铁钉(碳素钢)12.0 g放入30.0 mL浓硫酸中,加热充分反应后得到溶液X,并收集到气体Y。
(1)甲同学认为X中除Fe3+外还可能含有Fe2+。若要确认其中是否含有Fe2+,应选择加入的试剂为________(选填序号)
a.KSCN溶液和氯水? b.铁粉和KSCN溶液
c.浓氨水? d.酸性KMnO4溶液
(2)乙同学取672mL(标准状况)气体Y通入足量溴水中,发生反应:SO2+Br2+2H2O===2HBr+H2SO4,然后加入足量BaCl2溶液,经适当操作后得干燥固体4.66 g。由此推知气体Y中SO2的体积分数为___________。
【探究二】分析上述实验中SO2体积分数的结果,丙同学认为气体Y中还可能含有H2和CO2气体。为此设计了下列探究实验装置(图中夹持仪器省略)。

(3)写出产生CO2的化学方程式______________________________________
(4)装置A中试剂的作用是_____________________装置G的作用是??
(5)简述确认气体Y中含有CO2的实验现象___________________________。
(6)如果气体Y中含有H2,预计实验现象应是_________________________。
2、计算题 3.84克铜与足量的浓硫酸在加热条件下充分反应。
(1) 求生成的气体在标准状况下的体积是多少?
(2) 求被还原的硫酸的物质的量是多少?
(3) 将生成物稀释到500mL,求所得溶液中CuSO4的物质的量浓度是多少?
3、实验题 (18分)某校化学兴趣小组为研究Cu与浓硫酸反应并制备少量硫酸铜,进行如下实验。
该小组同学在实验中发现使用教材所提供的铜和浓硫酸反应的实验装置不仅安全性差而且易造成环境污染。经过同学们的讨论以及老师的指导,该小组设计了如图所示的装置并进行实验。
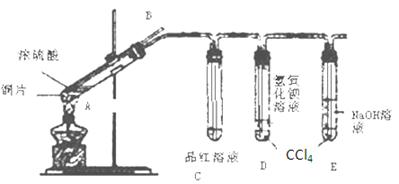
请回答:
(1)请写出长导管B的作用?(只写一点就可);
(2)写出检查该装置气密性的方法?。
(3)D、E试管中CCl4的作用?。
(4)写出A中发生反应的化学方程式并标出电子转移的方向与数目?
?
(5)对试管A进行加热,发现E试管中有气泡逸出,品红溶液很快褪色,但最终未见D试管中氢氧化钡溶液出现浑浊,为探究D试管中未出现浑浊的原因,该小组同学在化学手册中只查阅到下列物质常温下的溶解度数据:
物质
| 溶解度(g/100水)
| 物质
| 溶解度(g/100水)
|
Ca(OH)2
| 0.173
| Ba(OH)2
| 3.89
|
CaCO3
| 0.0013
| BaSO3
| 0.016
|
Ca(HCO3)2
| 16.60
| ?
| ?
|
请你应用类比研究方法帮他们预测D试管未出现浑浊的原因:?。
(6)为验证D试管中溶液的组成,进行了下列实验,请你帮助完成下列实验报告:
实验方案
| 现象
|
方案1:取少量溶液于试管中,加入稀盐酸,加热,用①检验产生的气体。
| ②?
|
方案2:取少量溶液于试管中,加入③?溶液并观察现象。
| ④?
4、实验题 (18分)某同学用如下图1所示的装置来探究SO2的性质及有关实验。
(1)实验前应先检验装置的气密性,方法是?
(2)实验室用亚硫酸钠固体与硫酸反应制取SO2气体,写出该反应的化学方程式
?。
(3)分别将SO2气体通入气体下列C溶液中,请回答下列问题:
①少量SO2通入紫色石蕊试液,现象是?,继续通入过量的SO2气体,现象是?。
②SO2通入紫红色KMnO4溶液,现象是?,
③SO2慢慢通入澄清石灰水中,现象?。
(4)若同学制取的SO2气体中混有CO2气体,请你设计实验证明混合气体中既有SO2气体,又有CO2气体。可以选择下图2洗气装置设计实验。洗气装置里的溶液是:
A浓硫酸、B氢氧化钠溶液、C硫酸铜溶液、D品红溶液、
E澄清石灰水、F高锰酸钾溶液、G碳酸氢钠溶液。
上述装置的所装试剂连接顺序是(用字母表示,所给装置可以重复使用,有些装置也可以不用)?。
5、选择题 浓H2SO4可以用来干燥H2、O2等气体,是由于浓H2SO4具有?(?)
A.吸水性
B.氧化性
C.酸性
D.脱水性
|