| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学必备知识点《物质的量》高频考点强化练习(2019年最新版)(六)
参考答案:D 本题解析:A、质量的单位是g,错误;B、摩尔质量的单位是g/mol,错误;C、未指明标准状况,所以44g二氧化碳的物质的量是1mol,1mol二氧化碳的体积不一定是22.4L,错误;D、9.8g H2SO4物质的量是9.8g/98g/mol=0.1mol,1个H2SO4分子中含有4个O原子,则O原子的物质的量是0.4mol,1mol物质的粒子数是NA,所以9.8g H2SO4含0.4NA个氧原子,正确,答案选D。 本题难度:一般 3、选择题 下列有关气体的体积叙述正确的是 参考答案:D 本题解析:A错 标况下,1mol任何气体的体积都约为22.4L 本题难度:简单 4、选择题 有一真空瓶质量为m1,该瓶充入空气后质量为m2。在相同状况下,若改为充入某气体A时,总质量为m3。已知空气的平均相对分质量为29,则A的相对分子质量是 ( ) |
参考答案:A
本题解析:真空瓶质量为m1,该瓶充入空气后质量为m2.令气体的物质的量为n,则:m1g+n×29g/mol=m2g,n=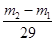 ,在相同状况下,若改为充入某气体A时,总质量为m3.所以A的质量为(m3-m1)g,物质的量为
,在相同状况下,若改为充入某气体A时,总质量为m3.所以A的质量为(m3-m1)g,物质的量为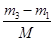 ,同温同压下,空气和A气体的物质的量相等,故
,同温同压下,空气和A气体的物质的量相等,故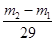 =
=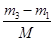 ,M=29
,M=29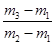 ,答案选A.
,答案选A.
考点:物质的量的有关计算
本题难度:一般
5、选择题 若以w1和w2分别表示物质的量浓度为c1 mol・L-1和c2 mol・L-1硫酸溶液的质量分数,已知2 w1=w2,则下列推断正确的(硫酸的密度比纯水的大) ( )
A.2c1=c2
B.2c2=c1
C.c2>2c1
D.c1<c2<2c1
参考答案:C
本题解析:浓硫酸的密度大于水,溶液的浓度越大,密度越大,利用c=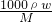 进行判断。设物质的量是浓度为c1 mol?L-1的密度为ρ1,物质的量是浓度为c2mol?L-1硫酸溶液的密度为ρ2,则c1=
进行判断。设物质的量是浓度为c1 mol?L-1的密度为ρ1,物质的量是浓度为c2mol?L-1硫酸溶液的密度为ρ2,则c1= ,c2=
,c2= ,
,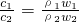 =
= 因浓硫酸的密度大于水,溶液的浓度越大,密度越大,则ρ1<ρ2,则c2>2c1,选C.
因浓硫酸的密度大于水,溶液的浓度越大,密度越大,则ρ1<ρ2,则c2>2c1,选C.
考点:考查物质的量浓度与质量分数的计算与比较
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学知识点归纳《物质的检验.. | |