1、选择题 在Ba(NO3)2、AgNO3、Cu(NO3)2溶液中分别滴入一种试剂都有沉淀产生.该试剂可能是( )
A.盐酸
B.硫酸
C.Na2CO3溶液
D.NaOH溶液
参考答案:A.加入盐酸,只生成AgCl沉淀,故A错误;
B.加入硫酸,硫酸铜溶于水,不是沉淀,故B错误;
C.加入Na2CO3溶液,分别生成BaCO3、Ag2CO3、CuCO3沉淀,故C正确;
D.加入NaOH溶液,只生成AgOH、Cu(OH)2沉淀,故D错误.
故选C.
本题解析:
本题难度:简单
2、填空题 阅读下表中短周期主族元素的相关信息。 请回答

(1)在一定条件下,B2与C的单质在海水中可形成原电池,为新型海水航标灯提供能源。写出该原电池正极的电极反应式_____________
(2)用惰性电极电解化合物AD的水溶液,该反应的化学方程式为:_________;其中,阴极产物是__________
(3)常温下,0.1 mol・L-1 X溶液的pH_________7(填“>”“=”或“<”),原因是 _____________(用离子方程式说明)。
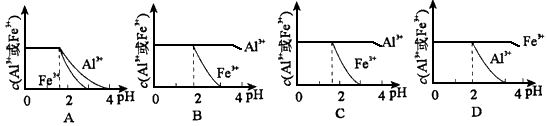
(4)已知Ksp[Al(OH)3]=1.3×10-33,Ksp[Fe(OH)3]=4.0×10 -38。现向pH=0,浓度均为0.04 mol・L-1的Al3+ 、Fe3+溶液中加入A的最高价氧化物对应水化物的溶液,以调节pH(设溶液体积不变),该过程中Al3+、Fe3+的浓度与pH关系正确的是______________(填字母代号)。
参考答案:(1)O2+4e-+2H2O=4OH-
(2) 2NaCl+ 2H2O=2NaOH+Cl2↑+H2↑ ;H2和NaOH
(3)> ;ClO-+H2O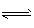 HClO+OH-
HClO+OH-
(4) B
本题解析:
本题难度:一般
3、简答题 向BaCl2溶液中先后滴加AgNO3和KBr,当两种沉淀共存时,
=______.[KSP(AgBr)=5.4×10-13,KSP(AgCl)=2.0×10-10].
参考答案:当两种沉淀共存时,溶液中Ag+离子浓度相同,根据溶度积常数计算,c(Br-)=Ksp(AgBr)c(Ag+),c(Cl-)=Ksp(AgCl)c(Ag+),
则c(Br-)c(Cl-)=Ksp(AgBr)Ksp(AgCl)=5.4×10-132.0×10-10=2.7×10-3;
故答案为:2.7×10-3.
本题解析:
本题难度:一般
4、选择题 某温度时,Ag2SO4在水溶液中的沉淀溶解平衡曲线如图所示:下列有关Ag2SO4说法正确的是
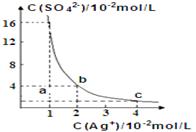
A.含有大量SO42-的溶液中肯定不存在Ag+
B.Ag2SO4的溶度积常数(Ksp)为8×10-4
C.a点表示Ag2SO4的不饱和溶液,蒸发可以使溶液由a点变到b点
D.0.02mol?L-1的AgNO3溶液与0.2mol?L-1的Na2SO4溶液等体积混合不会生成沉淀