1、选择题 用0.01 mol/L? H2SO4滴定0.01mol/L NaOH溶液,中和后加水至100ml,若滴定时终点判断有误差:①多加1滴H2SO4;②少加1滴H2SO4;(设1滴为0.05ml)则①和②c(H+)的比值是
A.10
B.50
C.5×103
D.104
参考答案:D
本题解析:多加1滴硫酸,则溶液中氢离子的浓度为 。同样少加1滴硫酸,溶液中OH-的浓度就应该是10-5mol/L,则①和②c(H+)的比值是104。答案选D。
。同样少加1滴硫酸,溶液中OH-的浓度就应该是10-5mol/L,则①和②c(H+)的比值是104。答案选D。
本题难度:一般
2、选择题 常温下,用0.1000 mol・L-1 NaOH溶液分别滴定20.00 mL 0.1000 mol・L-1盐酸和20.00 mL 0.1000 mol・L-1醋酸溶液,得到两条滴定曲线,如下图所示,若以HA表示酸,下列说法正确的是
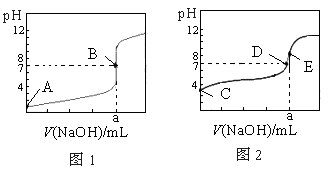
A.滴定盐酸的曲线是图2
B.达到B、E状态时,反应消耗的n(CH3COOH)>n(HCl)
C.达到B、D状态时,两溶液中离子浓度均为c(Na+)=c(A-)
D.当0 mL<V(NaOH)<20.00 mL时,对应混合液中各离子浓度大小顺序为c(A-)>c(Na+)>c(H+)>c(OH-)
参考答案:C
本题解析:A、滴定开始时0.1000mol/L盐酸pH=1,而0.1000mol/L醋酸pH>1,所以滴定盐酸的曲线是图1,故A不正确;B、达到B、E状态时,消耗的氢氧化钠物质的量是相等的,根据反应原理:HCl~NaOH,CH3COOH~NaOH,反应消耗的n(CH3COOH)=n(HCl),故B错误;C、达到B、D状态时,溶液是中性的,此时c(H+)=c(OH-),根据电荷守恒:c(Na+)+c(H+)=c(A-)+c(OH-),则两溶液中离子浓度均为?c(Na+)=c(A-),故C正确;D、当0?mL<V(NaOH)<20.00?mL时,酸相对于碱来说是过量的,所得溶液是生成的盐和酸的混合物,假设当加入的氢氧化钠极少量时,生成了极少量的钠盐(氯化钠或是醋酸钠),剩余大量的酸,此时c(A-)>c(H+)>c(Na+)>c(OH-),故D错误,答案选C。
本题难度:一般
3、选择题 室温下,用0.100 mol/L NaOH 溶液分别滴定20.00 mL 0.100 mol/L的盐酸和醋酸,
下列说法正确的是(?)
A.起始时盐酸和醋酸溶液PH相同
B.V(NaOH)=10.00 mL 时,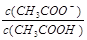 <1
<1
C.pH=7时,两种酸所用NaOH溶液体积不相等,醋酸用的体积多
D.V(NaOH)="20" .00 mL 时,c(Cl?)>c(CH3COO―)
参考答案:D
本题解析:A.盐酸和醋酸溶液的物质的量浓度相同,但是由于HCl是强酸,完全电离,CH3COOH是弱酸,部分电离,起始时盐酸和醋酸溶液PH不相同。错误。B.V(NaOH)=10.00 mL 时溶液为CH3COOH和CH3COONa等浓度的混合溶液。溶液中由于CH3COOH的电离作用大于CH3COO-的水解作用,所以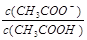 >1.错误。C.由于醋酸是弱酸,与NaOH反应得到的CH3COONa会发生水解发生消耗水电离产生的H+,使溶液显碱性。所以为了使溶液的pH=7,加入的NaOH就应该比强酸HCl要少些。错误。D.V(NaOH)="20" .00 mL 时,根据物料守恒可得c(Na+)=c(Cl?)=c(CH3COO―)+c(CH3COOH)。所以c(Cl?)>c(CH3COO―)。正确。
>1.错误。C.由于醋酸是弱酸,与NaOH反应得到的CH3COONa会发生水解发生消耗水电离产生的H+,使溶液显碱性。所以为了使溶液的pH=7,加入的NaOH就应该比强酸HCl要少些。错误。D.V(NaOH)="20" .00 mL 时,根据物料守恒可得c(Na+)=c(Cl?)=c(CH3COO―)+c(CH3COOH)。所以c(Cl?)>c(CH3COO―)。正确。
本题难度:一般
4、选择题 25℃时,amol/L稀盐酸与bmoL/L稀氢氧化钠溶液等体积混合后,所得溶液的pH=12(混合液的总体积可视为原两种溶液体积相加),则a和b的关系为(?)。
A.a=b/2
B.b=a+0.02
C.a=b+0.02
D. a=b+0.01
参考答案:B
本题解析:所得溶液的pH=12,即:[OH-]=1.0×10-2mol・L-1;
HCl+NaOH=NaCl+H2O
1? 1
aV? aV
[OH-]=(bV- aV)moL/2VL=1.0×10-2mol・L-1,得:b=a+0.02
本题难度:一般
5、选择题 25℃时,a mol・L-1一元酸HA与b mol・L-1NaOH等体积混合后pH=7,则下列关系一定正确的是? (? )
A.a=b
B.a>b
C.c (A-)= c(Na+)
D.c (A-)< c(Na+)
参考答案:C
本题解析:
A只是可能正确,若一元酸HA为弱酸,则a>b,故错
B也是可能正确,HA是强酸的情况下,两者混合后溶液呈酸性pH<7,故错
C溶液反应后pH=7就是呈中性。那么[H+]=[OH-],HA与NaOH反应后,溶液中的离子就只有Na+、H+、OH-、A-,因为溶液呈现的是电中性,所以[Na+]+[H+]=[OH-]+[A-]
[H+]=[OH-],代入上式,就得[Na+]=[A-],所以C一定正确,那么D就不正确了。
点评:本题属于中等题,难度不大,做题时要考虑全面,一元酸HA既可能是强酸也可能是弱酸,分两种情况讨论。
本题难度:一般