1、选择题 下列说法中,不正确的是( )
A.配位键也是一种静电作用
B.配位键实质上也是一种共价键
C.形成配位键的电子对由成键双方原子提供
D.配位键具有饱和性和方向性
参考答案:C
本题解析:试题分析:形成配位键的电子对由单方原子提供,所以选项C不正确,其余选项都是正确的,答案选C。
考点:考查配位键的有关判断
点评:该题是基础性知识的考查,试题注重基础和能力的双向考查。该题的关键是明确配位键的含义、形成条件,然后结合题意灵活运用即可,有利于培养学生的逻辑思维能力。
本题难度:困难
2、选择题 下列含有同一元素的含氧酸中酸性强弱比较正确的是
A.H2SO3>H2SO4
B.HNO3>HNO2
C.H3PO3>HPO3
D.HClO>HClO4
参考答案:BC
本题解析:同种元素的不同价态的无机含氧酸,价态越高,酸性越强。
本题难度:简单
3、选择题 我国在砷化镓太阳能电池研究方面国际领先。砷(As)和镓(Ga)都是第四周期元素,分别属于ⅤA和ⅢA族。下列说法中,不正确的是
A.原子半径:Ga > As > P
B.热稳定性:NH3 > PH3 > AsH3
C.酸性:H3AsO4 > H2SO4 > H3PO4
D.Ga(OH)3可能是两性氢氧化物
参考答案:C
本题解析:试题分析:根据原子半径下大于上,左大于右,和Ga、As、P在周期表中的位置,可知原子半径:Ga > As > P,A正确。根据非金属性越强,气态氢化物越稳定,可知热稳定性:NH3 > PH3 > AsH3,B正确。根据非金属性越强,最高价氧化物对应水化物的酸性越强,可知酸性:H2SO4 > H3PO4> H3AsO4,C错误。Al与Ga同族,Al(OH)3是两性氢氧化物,Ga(OH)3可能是两性氢氧化物,D正确。答案选C。
考点:元素周期律
点评:元素的性质随着原子序数的递增而呈现周期性的变化,称为元素周期律。元素周期律需要熟练记住,但关键是利用好元素周期律解决实际问题。
本题难度:一般
4、选择题 X、Y、Z都是第三周期元素,核电荷数依次增大,X的氧化物对应水化物为强碱,Z的原子半径最小。据此判断下列说法不正确的是
A.X是第ⅠA元素,Z是第ⅦA元素
B.X、Y、Z三种元素的最高化合价依次升高
C.Z的最高价氧化物对应的水化物是强酸
D.如果Y的最高价氧化物的水化物难溶于水,则Y一定是Al
参考答案:D
本题解析:同周期自左向右原子半径逐渐减小,金属性逐渐减弱,非金属性逐渐增强。所以根据元素的性质及位置可知,Z是氯元素,选项ABC都是正确的。D中Y也可能是镁元素,不正确。答案选D。
本题难度:一般
5、选择题 下列化合物中不含离子键的是
A.(NH4)2S
B.Al2(SO4)3
C.CsOH
D.HNO3
参考答案:D
本题解析:(NH4)2S和Al2(SO4)3都是盐,CsOH是强碱,它们都是离子化合物,都含离子键。
HNO3属于酸,HNO3溶于水也能电离出H+和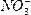 ,但HNO3是共价化合物,分子中不含离子键。
,但HNO3是共价化合物,分子中不含离子键。
本题难度:简单