| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学知识点总结《化学平衡状态的判断》考点预测(2019年强化版)(十)
a.请在上表空格中填入剩余的实验条件数据。 b.根据反应II的特点,在给出的坐标图中,画出在5MPa条件下CO的转化率随温度变化的趋势曲线示意图,并标明压强。 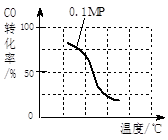 参考答案:(1)①0.003mol/(L・min)(2分)?②<(2分)2.25×10-4(3分) ? 本题解析:⑴①0.003mol/(L・min)?②<2.25×10-4?⑵③反应Ⅱ为熵减的反应,要自发反应必须为放热反应,故△H?<?0,若容器容积不变,可增加甲醇产率的措施有BD。④a通过“控制变量法”探究外界条件对化学平衡的影响,探究的前提只能是改变一个条件,而其它条件不变,由此可得:Ⅱ中温度为150℃,n?(CO)/n(H2)=1/3,Ⅲ中n?(CO)/n(H2)为1/3; 本题难度:困难 4、选择题 对于密闭容器中进行的可逆反应:2SO2(g)+O2(g)?2SO3(g),下列能判断该反应已经达到化学平衡状态的是( ) 参考答案:A、SO2、O2、SO3的浓度相等,正逆反应速率不一定相等,故A错误; 本题解析: 本题难度:简单 5、选择题 在密闭容器中,aA(g) 参考答案:AC 本题解析:若平衡不移动,A、B的浓度减为原来的一半,现B的浓度变为原来的60%,说明平衡向生成B的方向(正反应方向)移动,A的转化率增大,减压向正反应方向移动,说明正反应方向气体物质的量增加,则 本题难度:一般 |
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学知识点总结《分子式、结.. | |