1��ѡ���� �����й��������������˵���У���ȷ���ǣ���������
A������¯�г�����¯������ֱ�ӽ���ת�����н��д�����
B������������ķ�Ӧ�У�����������Ψһ����������
C������������Ҫ���ø��¸�ѹ���������ڶ���������õ�ת��Ϊ��������
D�������������������б�����ʱ��ͨ������������Ϊ98.3%�����������ռ�������ֱ����ˮ����
�ο��𰸣�D
������������������������������ԭ��������¯�г�����¯�����˺���SO2��O2��N2���ˮ�������������ʣ�ˮ���������ʶ��豸����һ�����е�������Ӧ�к�����˱�����о������ﴦ������A����FeS2����������������ΪSO2��Fe2O3����B�����¶Է�Ӧ��������������ת���ʲ�������ѹ��Ȼ�Զ��߽���������ʵ��֤����ѹ�¶�������ת�����Ѿ��ܸߣ���C��������������98.3%�����������ռ������Է�ֹ�γ����������������������ʣ���D��ȷ��
�����Ѷȣ���
2��ѡ���� ��6.4��CuͶ�뵽һ������������Һ�У�Cuȫ���ܽ⣬��Һ��ʣ��H+amol����Һ�к�NO3-�����ʵ���Ϊmol��
A.0.2
B.a
C.0.2+a
D.����ȷ��
�ο��𰸣�C
�������������������Cu+4HNO3�TCu��NO3��2+2NO2��+2H2O��3Cu+8HNO3�T3Cu��NO3��2+2NO��+4H2O������Cu��NO3��2��Cu��NO3-�Ĺ�ϵ��ʣ��������������
�����CuͶ�뵽һ������������Һ�У�����Cu+4HNO3�TCu��NO3��2+2NO2��+2H2O��3Cu+8HNO3�T3Cu��NO3��2+2NO��+4H2O��
��֪Cu��2NO3-��
n��Cu��=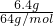 =0.1mol��
=0.1mol��
����Һ��n��NO3-��=0.1mol��2=0.2mol��
����Һ��ʣ��H+amol����ʣ��������n��NO3-��=amol��
���Է�Ӧ����Һ��n��NO3-��=amol+0.2mol=��0.2+a��mol��
��ѡC��
���������⿼������Ļ�ѧ���ʣ���ȷ��Ӧ��Cu����������ӵĹ�ϵ�ǽ����Ĺؼ����ѶȲ���
�����Ѷȣ���
3��ѡ���� ������ѧ��ŵ�������Ƴ�һ�ֿ��Խ�ˮ�ֽ�������������Ĵ������⽫ʹ����������Ϊ���ܣ���ʹ̫����ʹ�ò����µ�ʱ��������Ϊ��ˮ���缼�����������й�˵����ȷ���ǣ���������
A����ˮ���缼������ָˮ�ֽ�����������������ͬʱ�ų�����������
B����ˮ���缼����������ת����ʽΪ����ѧ�ܡ����ܡ�����
C����ˮ�ֽ������H2��O2�ֱ�ͨ��ȼ�ϵ�ص�������ͨH2�ļ�Ϊ��Դ����
D����ˮ���缼������ʵ�ַ�������е����ŷ�
�ο��𰸣�D
���������A��ˮ�ֽ�Ĺ��������ȹ��̣�A˵������B�ˮ���缼����������ת����ʽΪ̫���ܡ���ѧ�ܡ����ܣ�C������ȼ�ϵ���У�ͨH2��Ϊ��Դ������D����ȷ��
�����Ѷȣ���
4������� (15��)�Ȼ���ͭ��CuCl�����л��ϳɹ�ҵ��Ӧ�ýϹ㷺�Ĵ��������ǰ�ɫ��ĩ������ˮ���������Ҵ����ڿ����лᱻѸ�������������Ե�Ʒ�Һ����Ҫ��Cu2+��Fe3+�����Ʊ��Ȼ���ͭ�Ĺ�������ͼ���£�
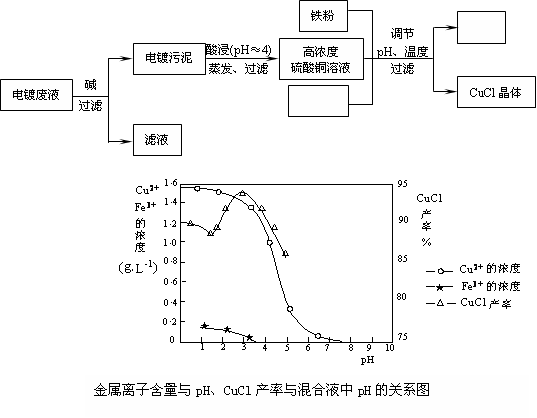
��ش��������⣺
��1������������Ҫ�ɷ���?��д��ѧʽ����
��2�����ʱ������Ӧ�����ӷ���ʽ��?��
��3������CuCl����ʱ�����pH��?���ң�
��4�����ۡ��Ȼ��ơ�����ͭ����Һ�з�Ӧ����CuCl�����ӷ�Ӧ����ʽΪ��
?��
��5��������CuCl����Ҫ��������ˮ�Ҵ�ϴ�ӣ�Ȼ����ո����ȴ���ܷ��װ����ո���ܷ��װ��Ŀ����?��
�ο��𰸣���(1��Cu(OH)2? Fe(OH)3����2�֣�?��2��Cu(OH)2+2H+= Cu2++2H2O��3�֣�
��3��3��2�֣�?��4��2Cu2++2Cl�D+ Fe��2CuCl��+ Fe2+��3�֣�
4.�ӿ��Ҵ���ˮ����������ֹCuCl������������3�֣�
�������������1������������Ҫ�ɷ���Cu(OH)2?Fe(OH)3, ���ʱ������Ӧ�����ӷ���ʽ��Cu(OH)2+2H+= Cu2++2H2O, ����CuCl����ʱ�����pH��3���ҡ���ո���ܷ��װ��Ŀ���Ǽӿ��Ҵ���ˮ����������ֹCuCl������������
�����Ѷȣ�һ��
5��ѡ���� 2013���ŵ������ѧ���ٴ�������㻯ѧ����Ŀ�ѧ�ҡ����»��ڽṹ���۽��з��Ѽ���ó�����
A����Ȼ������ֵ
B���ϳɰ���ԭ��������
C�����صĺ�����
D��p��������Ƶ���״
�ο��𰸣�D
���������2013��10��9�գ�2013��ŵ������ѧ��������������̫���������ۻ�ѧ��������������˹(Martin Karplus)������˹̹����ѧ��������ѧ�����˶�����ά��(Michael Levitt)���ϼ��ݴ�ѧ��ѧ������Ү����л��(Arieh Warshel)������ӻ�ѧ��ϵ����˶�߶�ģ�Ͷ�������������ṩ�𰸣�D��ȷ��
�����Ѷȣ���