1、简答题 根据以下叙述,回答1~2小题.
1995年诺贝尔化学奖授予致力于研究臭氧层被破坏问题的三位环境化学家.大气中的臭氧层可滤除大量的紫外光,保护地球上的生物.氟利昂(如CCl2F2可在光的作用下分解,产生Cl原子,Cl原子会对臭氧层产生长久的破坏作用(臭氧的分子式为O3).有关反应为:O3
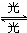
O2+O Cl+O3→ClO+O2 ClO+O→O2 总反应?2O3→3O2在上述臭氧变成氧气的反应过程中,Cl是( )
A.反应物
B.生成物
C.中间产物
D.催化剂
参考答案:总反应方程式2O3→3O2,臭氧是反应物,氧气是生成物.
A、该反应的反应物是O3,故A错误;
B、该反应的生成物是氧气,故B错误;
C、反应物中不含氯元素,氯原子不是中间产物,故C错误;
D、从反应历程看,第二、三两步反应氯原子在反应前后组成与质量都不变,所以是催化剂,故D正确;
故选D.
本题解析:
本题难度:一般
2、选择题 下列说法中错误的是( )
A.加热一般能加快化学反应速率
B.粉碎固体物质能加快化学反应速率
C.不同物质的化学反应速率可能不一样
D.化学方程式中各物质的化学反应速率之比等于其质量比
参考答案:A.加热可使反应的活化分子的百分数增大,反应速率增大,故A正确;
B.粉碎固体物质,固体表面积增大,反应速率增大,故B正确;
C.反应速率之比等于化学计量数之比,不同物质表示的反应速率的大小可能不同,故C正确;
D.化学方程式中各物质的化学反应速率之比等于化学计量数之比,故D错误.
故选:D.
本题解析:
本题难度:简单
3、选择题 在相同体积的密闭容器中,按照如下条件充入反应混合物,开始反应时速率最小的是( )
A.400℃10mol SO2?和5molO2
B.400℃20mol SO2?和5molO2
C.300℃10mol SO2?和5molO2
D.300℃20mol SO2?和10molO2
参考答案:A与B相比,B中SO2的物质的量大,即SO2的浓度大,其它条件相同,浓度越大,反应速率越快,所以反应速率:B>A;
C与D相比,D中SO2的物质的量比B中大,即SO2的浓度比C中大,其它条件相同,浓度越大,反应速率越快,所以反应速率:D>C;
A与C相比,其它条件相同,A中温度高,温度越高,反应速率越快,所以反应速率:A>C;
所以开始反应时速率最小的是C.
故选:C
本题解析:
本题难度:一般
4、选择题 对于反应:NO+CO2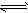 NO2+CO在体积可变的密闭容器中进行,下列条件改变能加快该反应速率的是
NO2+CO在体积可变的密闭容器中进行,下列条件改变能加快该反应速率的是
[? ]
A.扩大容器体积
B.体积不变充入CO2
C.体积不变充入He气
D.压强不变充入N2
参考答案:B
本题解析:
本题难度:一般
5、选择题 100mL?6mol?L-1?H2SO4?跟足量锌粉反应,在一定温度下,为了减缓反应进行的速率,但又不影响生成氢气的总量,可向反应物中加入适量的( )
A.碳酸钠固体
B.硝酸钠
C.硫酸钾固体
D.醋酸钠固体
参考答案:A.加入碳酸钠固体,与硫酸反应,导致反应物浓度降低,反应速率减小,但硫酸物质的量减小,影响生成氢气的总量,故A错误;
B.加入硝酸钠,在酸性条件下,NO3-具有强氧化性,与Zn反应生成NO,不生成氢气,故B错误;
C.加入硫酸钾固体,溶液浓度不变,反应速率和氢气的总量都不受影响,故C错误;
D.加入醋酸钠固体,生成弱电解质醋酸,溶液氢离子浓度减小,反应速率减小,但不影响生成氢气的总量,故D正确.
故选D.
本题解析:
本题难度:一般