1������� ��15�֣�ij��ѧС��Ϊ���о���������Ի�ѧ��Ӧ���ʵ�Ӱ�죬����������ʵ�飺
��ʵ��ԭ����2KMnO4 + 5H2C2O4 + 3H2SO4�� K2SO4 + 2MnSO4 + 10CO2�� + 8H2O
��ʵ�����ݼ���¼��
ʵ����
| �����£��Թ��������Լ��������� / mL
| ��������Һ��ɫ������ɫ����ʱ�� / min
|
0.6 mol/L
H2C2O4��Һ
| H2O
| 3 mol/L
ϡ����
| 0.05mol/L KMnO4��Һ
|
1
| 3.0
| 2.0
| 2.0
| 3.0
| 1.5
|
2
| 2.0
| 3.0
| 2.0
| 3.0
| 2.7
|
3
| 1.0
| 4.0
| 2.0
| 3.0
| 3.9
|
��ش�
��1�������ϱ��е�ʵ�����ݣ����Եõ��Ľ����� ��
��2������ʵ��1�����ݼ��㣬����KMnO4��Ũ�ȱ仯��ʾ�ķ�Ӧ����Ϊ����(KMnO4)�� ��
��3����С��ͬѧ���ݾ��������n(Mn2+) ��ʱ��仯���Ƶ�ʾ��ͼ����ͼ1��ʾ������ͬѧ�������е�ʵ�����Ϸ��֣���ʵ�������n(Mn2+) ��ʱ��仯������Ӧ��ͼ2��ʾ����С��ͬѧ����ͼ2��ʾ��Ϣ������µļ��裬����������ʵ��̽����

�ٸ�С��ͬѧ����ļ����� ��
�����������С��ͬѧ���ʵ�鷽��������д���пհס�
ʵ����
| �����£��Թ��������Լ��������� / mL
| �����Թ��м�����������
| ��������Һ��ɫ������ɫ����ʱ�� / min
|
0.6 mol/L
H2C2O4��Һ
| H2O
| 3 mol/L
ϡ����
| 0.05 mol/L KMnO4��Һ
|
4
| 3.0
| 2.0
| 2.0
| 3.0
|
| t
|
������С��ͬѧ����ļ��������Ӧ�۲쵽�������� ��
��4����ҵ�Ͽ��õ��K2MnO4Ũ��Һ�ķ�����ȡKMnO4������ʱ�����������ĵ缫��ӦΪ ���ܷ���ʽΪ ��
�ο��𰸣���1������������ͬʱ������H2C2O4Ũ�ȣ���Ӧ��Ũ�ȣ�����Ӧ��������3�֣�ÿ��1�֣�
��2��1.0��10��2 mol / (L��min) ��2�֣�
��3�� ���������е�MnSO4Ϊ�÷�Ӧ�Ĵ�������Mn2+�Ը÷�Ӧ�д����ã�[2�֣���ָ��MnSO4����Mn2+����1��] �� MnSO4 ��2�֣�
�� ��ʵ��1�Ƚϣ���Һ��ɫ����ʱ��̣�2�֣���д����ʵ��1�Ƚϡ���1�֣� ������ʱ�䣨t��С��1.5min�������������𰸣�
��4��2MnO42����2e����2MnO4������ MnO42����e����MnO4�� �� ��2�֣���
2K2MnO4+2H2O���2KMnO4+2KOH+H2����2�֣�
�����������1�����ݱ������ݿ�֪������������ͬʱ������H2C2O4Ũ�ȣ���Ӧ��Ũ�ȣ�����Ӧ��������
��2����Ӧ�����ĸ�����ص�Ũ����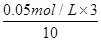 ��0.015mol/L�����Ԧ�(KMnO4)��0.015mol/L��1.5min��1.0��10��2 mol / (L��min)��
��0.015mol/L�����Ԧ�(KMnO4)��0.015mol/L��1.5min��1.0��10��2 mol / (L��min)��
��3������ͼ2��֪��Ӧ��ʼ����������ıȽϿ죬˵���������е�MnSO4����Mn2+��Ϊ�÷�Ӧ�Ĵ���.
��Ҫ��֤�������Ա�ʵ������ʵ��1�Ƚϣ�����������ͬʱ����MnSO4���ɡ�
��������������������������Ժ�����Ӧ�ӿ죬��Һ��ɫ��ʱ��С��1.5min��˵��Mn2+�Ǵ���.
��4��K2MnO4��ȡKMnO4����Ӧ������MnԪ�صĻ��ϼ۴�+6�����ߵ�+7�ۣ����������������ŵ磬�缫��ӦʽΪMnO42����e����MnO4������������Һ�е������ӷŵ���������������ܷ�ӦʽΪ2K2MnO4+2H2O���2KMnO4+2KOH+H2����
���㣺���鷴Ӧ���ʼ��㡢��������Է�Ӧ���ʵ�Ӱ���Լ����ԭ����Ӧ��
�����Ѷȣ�һ��
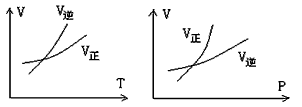
2��ѡ���� ���淴ӦmA(g)  nB(g)+ pC(s)���¶Ⱥ�ѹǿ�ı仯�����淴Ӧ���ʵ�Ӱ��ֱ����ͼ�е�����ͼ������������ȷ����
nB(g)+ pC(s)���¶Ⱥ�ѹǿ�ı仯�����淴Ӧ���ʵ�Ӱ��ֱ����ͼ�е�����ͼ������������ȷ����
[? ]
A��m��n������Ӧ����
B��m��n+p������Ӧ����
C��m��n������Ӧ����
D��m��n+p������Ӧ����
�ο��𰸣�A
���������
�����Ѷȣ�һ��
3��ѡ���� Ӱ�컯ѧ��Ӧ���ʵ������ж�棬��Ũ�ȡ�ѹǿ���¶ȡ������ȡ������й�˵������ȷ����
A���ı�ѹǿ�ܸı����巴Ӧ������
B������Ũ���ܼӿ컯ѧ��Ӧ���ʣ�ԭ��������Ũ�Ⱦ������˷�Ӧ��ϵ�л���ӵİٷ���
C���¶�����ʹ��ѧ��Ӧ���ʼӿ����Ҫԭ���������˷�Ӧ��ϵ�л���ӵİٷ���
D�������ܼӿ컯ѧ��Ӧ������Ҫԭ���ǽ��ͷ�Ӧ���������