1、选择题 决定化学反应速率的根本因素是
[? ]
A.温度和压强
B.反应物的浓度
C.参加反应的各物质的性质
D.催化剂的加入
参考答案:C
本题解析:
本题难度:简单
2、选择题 下图中,在某可逆反应达到平衡状态后,只升高温度时对化学反应速率影响的图象中,正确的是( )
A.

B.

C.
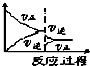
D.

参考答案:A、由图象可知,升温的瞬间逆反应速率不变,与升高温度正逆反应速率均增大相矛盾,故A错误;
B、由图象可知,升高温度正逆反应速率都增大,若逆反应为吸热反应,升高温度,化学平衡逆向移动,则逆反应速率大于正反应速率,故B正确;
C、由图可知,升高温度,正逆反应速率减小,与事实不符,故C错误;
D、由图象可知,升高温度时正逆反应速率均增大,但正逆反应速率不会同等程度的增大,与事实不符,故D错误;
故选B.
本题解析:
本题难度:简单
3、实验题 (9分)在室温下,将表面积相同、纯度相同、体积也相同的同种锌片分别投入lOOmL、O.1mol/L的稀硫酸和0.2mol/L的稀盐酸中,仔细观察后发现,两者反应速率有明显差异,投入到稀硫酸中的锌表面产生的气泡没有投人到稀盐酸中的快。大家分析、讨论后认为产生这一现象的原因可能有两个:氯离子对反应起了正的催化作用,即氯离子加快了反应;
另一种可能是硫酸根离子对反应起了负催化作用,即硫酸根离子阻碍了反应的进行。持前一种观点的三位同学设计实验并根据实验现象认为均证实了自己的推论是正确的,他们的实验方案和实验现象分别是:
甲:在室温下,将表面积相同、纯度相同、体积也相同的同种锌片投人lOOmL0.1mol/L的稀硫酸中,并加入适量氯化钠固体,发现反应速率加快;
乙:在室温下,将表面积相同、纯度相同、体积也相同的同种锌片投入lOOmLO.1mol/L的稀硫酸中,并加入适量氯化锌固体,发现反应速率加快;
丙:在室温下,将表面积相同、纯度相同、体积也相同的同种锌片投人lOOmLO.1moL/L的稀硫酸中,并加入适量氯化钡固体,发现反应速率加快;
请你对三位同学的实验方案作出评价,他们能否得出“氯离子对反应起了正的催化作用”的结论,并简要说出弹由.
甲:________;____________________________________________________________
乙:________;____________________________________________________________
丙:________;____________________________________________________________
参考答案:(9分,结论1分,理由2分)
甲:不能,因为可能是钠离子起了正催化作用;
乙:能,因为反应中均有锌离子生成,因此可以排除锌离子干扰,反应速率加快只能是氯离子起了正催化作用;
丙:不能,因为适量钡离子沉淀了硫酸根,反应速率加快也可能是因为排除了硫酸根离子的阻碍作用。
本题解析:①由于甲加入的是氯化钠,从而引入了钠离子,而钠离子也可能起了正催化作用,所以甲同学的结论是错误的。
②乙同学的结论是正确的,因为反应中均有锌离子生成,因此可以排除锌离子干扰,反应速率加快只能是氯离子起了正催化作用。
③在丙中由于生成硫酸钡沉淀,因此反应速率加快也可能是因为排除了硫酸根离子的阻碍作用而导致的。
本题难度:一般
4、选择题 一定条件下,分别对反应A(s)+B(g) 2C(g) (正反应吸热)进行如下操作(只改变该条件):
2C(g) (正反应吸热)进行如下操作(只改变该条件):
①增大A的用量 ②缩小容器的容积 ③升高体系温度 ④减小体系中C的量
上述措施中一定能使正反应速率加快的是
A.①③
B.②③
C.①②③
D.①②③④