|
高中化学知识点大全《弱电解质电离平衡》考点特训(2019年冲刺版)(六)
2020-07-07 23:43:29
【 大 中 小】
|
1、选择题 下列关于0.10 mol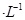 NaHSO3溶液的说法正确的是 NaHSO3溶液的说法正确的是
A.加入NaOH固体,溶液pH减小
B.温度升高,c(HSO3-)增大
C.25 C时,加水稀释后,n(H+)与n(OH-)的乘积变大 C时,加水稀释后,n(H+)与n(OH-)的乘积变大
D.NaHSO3的电离方程式为NaHSO3 = Na++H++SO32-
|
参考答案:C
本题解析:根据NaHSO3+NaOH=Na2SO3+H2O,加入NaOH固体,溶液PH增大,A项错误;HSO3-的电离过程和水解过程都是吸热过程,温度升高,电离过程增大,水解程度增大,c(HSO3-)减小,B项错误;在同一溶液中,n(H+)?n(OH-)=C(H+)?c(OH-)V×V=KwV×V,加水稀释,KW不变,V增大,则加水稀释后,n(H+)与n(OH-)的乘积变大,C项正确;钠盐是强电解质,电离方程式为NaHSO3 = Na++HSO3-,D项错误;选C。
考点:考查NaHSO3溶液中各种关系。
本题难度:一般
2、填空题 某二元酸(化学式用H2A表示)在水中的电离方程式是:
H2A=H++HA-,HA- H++A2- H++A2-
回答下列问题:
(1)Na2A溶液显________(填“酸性”“中性”或“碱性”),用离子方程式表示其原因
__________________________________________________
(2)在0.1 mol・L-1的Na2A溶液中,下列微粒浓度关系式正确的是________。
A.c(A2-)+c(HA-)+c(H2A)=0.1 mol・L-1
B.c(OH-)=c(H+)+c(HA-)+2c(H2A)
C.c(Na+)+c(H+)=c(OH-)+c(HA-)+2c(A2-)
D.c(Na+)>c(A2-)>c(HA-)>c(OH-)>c(H+)
(3)常温下,已知0.1 mol・L-1NaHA溶液的pH=2,则0.1 mol・L-1H2A溶液中c(H+)可能
______(填“>”、“<”或“=”)0.11 mol・L-1;理由是____________________________
(4)比较①0.1 mol・L-1 Na2A溶液 ②0.1 mol・L-1 Na2SO4溶液,两种溶液中阴离子总浓度的大小①________②(填“>”、“<”或“=”)。
参考答案:(1)碱性 A2-+H2O HA-+OH- HA-+OH-
(2)C
(3)< H2A一级电离出H+,对HA-电离起抑制作用,而NaHA中不存在抑制作用
(4)>
本题解析:(1)由题目所给信息HA- H++A2-,可知HA-具有弱酸性,Na2A能发生水解反应A2-+H2O H++A2-,可知HA-具有弱酸性,Na2A能发生水解反应A2-+H2O HA-+OH-,其溶液呈碱性。 HA-+OH-,其溶液呈碱性。
(2)由于H2A的第一步电离是完全的,故溶液中不存在H2A分子,A项、B项均不正确;根据电荷守恒? C项正确;D项溶液中各离子浓度大小关系应为:c(Na+)>c(A2-)>
c(OH-)>c(HA-)>c(H+),D项错误。
(3)由题意可知0.1 mol・L-1NaHA溶液中,
c(H+)=0.01 mol・L-1,即0.1 mol・L-1的HA-电离产生的c(H+)=0.01 mol・L-1。0.1 mol・L-1 H2A电离产生的c(H+)、c(HA-)均为0.1 mol・L-1,因产生的H+抑制HA-的电离,使溶液中H+的浓度小于0.11 mol・L-1。
(4)由于①Na2A溶液水解呈碱性:A2-+H2O HA-+OH-,1 mol A2-水解会生成2 mol阴离子HA-和OH-;②Na2SO4溶液不水解呈中性;故同样浓度的①、②两溶液,阴离子总浓度①>②。 HA-+OH-,1 mol A2-水解会生成2 mol阴离子HA-和OH-;②Na2SO4溶液不水解呈中性;故同样浓度的①、②两溶液,阴离子总浓度①>②。
本题难度:一般
3、选择题 在0.l mol・L-1的CH3COOH溶液中存在如下电离平衡:CH3COOH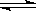 CH3COO-+H+,对于该平衡,下列叙述正确的是 CH3COO-+H+,对于该平衡,下列叙述正确的是
A.升温,平衡向正反应方向移动,溶液的pH值不变
B.加水,反应速率加快,平衡向逆反应方向移动
C.滴加少量0.lmol・L-1 HCl溶液,溶液中c(H+)减少
D.加入少量CH3COONa固体,平衡向逆反应方向移动
参考答案:D
本题解析:升高温度,促进电离,氢离子浓度增大,pH减小,A不正确;稀释促进电离,B不正确;加入盐酸,抑制醋酸的电离,但溶液中氢离子浓度增大,C不正确。D中增大CH3COO-浓度,抑制醋酸的电离,D正确,答案选D。
点评:该题是基础性试题的考查,主要是考查学生对醋酸电离平衡状态以及外界条件对醋酸电离平衡状态影响的了解掌握情况,旨在培养学生分析、归纳、总结问题的能力。有利于培养学生的逻辑推理能力和应试能力。
本题难度:一般
4、填空题 A、B、C、D、E五种溶液分别是NaOH、NH3・H2O、CH3COOH、HCl、NH4HSO4中的一种。常温下进行下列实验:
①将1 L pH=3的A溶液分别与0.001mol/L xL B溶液、0.001mol/L yL D溶液充分反应
②浓度均为0.1mol/LA和E溶液,pH:A<E
③浓度均为0.1 mol/LC与D溶液混合,溶液呈酸性。
回答下列问题:
(1)D是____溶液,判断理由是_______________
(2)用水稀释0.1mol/LB时,溶液中随着水量的增加而减小的是_________ (填写序号)。
①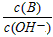 ?② ?②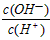 ③c(H+)和c(OH-)的乘积 ④OH-的物质的量 ③c(H+)和c(OH-)的乘积 ④OH-的物质的量
(3)OH-浓度相同的等体积的两份溶液A和E分别与锌粉反应,若最后仅有一份溶液中存在锌粉,且放出氢气的质量相同,则下列说法正确的是____(填写序号)。
①反应所需要的时间E>A ②开始反应时的速率A>E
③参加反应的锌粉物质的量A=E ④反应过程的平均速率E>A
⑤A溶液里有锌粉剩余?⑥E溶液里有锌粉剩余
(4)将等体积、等物质的量浓度B和C混合后溶液,升高温度(溶质不会分解)溶液pH随温度变化如图中的____曲线(填写序号)。
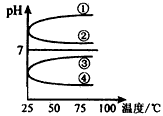
(5)室温下,向0.01 mol/L C溶液中滴加 0.01 mol・L-1D溶液至中性,得到的溶液中所有离子的物质的量浓度由大到小的顺序为_______________。
参考答案:(1)NaOH;中和酸性物质A只有NaOH、NH3・H2O,物质的量的A与等物质的量浓度B和D混合呈中性;
D的用量少,说明D碱性比B的碱性强,所以D是NaOH
(2)①②
(3)③④⑤
(4)④
(5)c(Na+)>c(SO42-)>c(NH4+)>c(H+)=c(OH-)
本题解析:
本题难度:困难
5、选择题 (2我c4?广州一模)对于常温下我.cmol?L-c氨水和我.cmol?L-c醋酸,下列说法正确的是( )
A.0.1mol?L-1氨水,溶液的pH=13
B.0.1mol?L-1氨水加水稀释,溶液中c(H+)和c(OH-)都减小
C.0.1mol?L-1醋酸溶液中:c(H+)=c(CH3COO-)
D.0.1mol?L-1醋酸与0.1mol?L-1 NaOH溶液等体积混合所得溶液中:c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
参考答案:A.一水合氨是弱电解质,在水溶液里部分电离,所以氨水溶液中存在一水合氨电离平衡,则0.3mo3?3-3氨水,溶液的pH<33,故A错误;
B.加水稀释促进一水合氨电离,氢氧根离子增多t数小于溶液体积增大倍数,所以溶液中氢氧根离子浓度减小,温度不变,水的离子积常数不变,则氢离子浓度增大,故B错误;
C.任何电解质溶液中都存在电荷守恒,根据电荷守恒得c(H+)=c(CH3COO-)+c(OH-),故C错误;
D.等物质的量的醋酸和氢氧化钠混合,二者恰好反应生成醋酸钠,醋酸钠为强碱弱酸盐,其溶液呈碱性c(OH-)>c(H+),根据电荷守恒得c(Na+)>c(CH3COO-),盐类水解较微弱,所以c(CH3COO-)>c(OH-),该溶液中离子浓度大小顺序是c(Na+)>c(CH3COO-)>c(OH-)>c(H+),故D正确;
故选D.
本题解析:
本题难度:一般
|