1��ѡ���� һ���¶��£���һ�ݻ�������ܱ������з����Ŀ��淴Ӧ2X(g)  Y(g)+Z(s)��������˵����Ӧ�ﵽƽ���־�ģ�?��
Y(g)+Z(s)��������˵����Ӧ�ﵽƽ���־�ģ�?��
A����������ѹǿ���ٱ仯
B��X��Y��Z�����ʵ���֮��Ϊ2��1��1
C����λʱ��������lmolY��ͬʱ�ֽ�2mol X
D��X�ķֽ�������Y�������������
2��ѡ���� ijһ��Ӧ��һ�������µ�ƽ��ת����Ϊ25.3%����ʹ���˴���ʱ����ת����Ϊ��?��
A������25.3%
B����25.3%
C������25.3%
D��Լ����25.3%
3��ѡ���� ��ҵ���õ����������ϳɰ���N2+3H2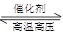 2NH3(��Ӧ����)���ӷ�Ӧ���ʺͻ�ѧƽ�������濴���ϳɰ�����������һ��Ϊѹǿ��20 MPa��50 MPa���¶ȣ�500 �����ң�����������ý�������йغϳɰ���ҵ����������ȷ����
2NH3(��Ӧ����)���ӷ�Ӧ���ʺͻ�ѧƽ�������濴���ϳɰ�����������һ��Ϊѹǿ��20 MPa��50 MPa���¶ȣ�500 �����ң�����������ý�������йغϳɰ���ҵ����������ȷ����
A��ʹ������ý����ʹ�����������������֮��ķ�Ӧ�ڽϵ��¶���ȡ�ýϸߵķ�Ӧ����
B����ҵ��ѡ�����������ºϳɰ�������ʹ����ȫ��ת��Ϊ��
C��������ѧƽ����ƶ��ܵ��¶ȡ���Ӧ���Ũ�ȡ�ѹǿ�����ص�Ӱ��
D���¶����ߣ������ڵ�����ת����
4������� �������ʵ�����A��B�����2L���ܱ������з�����Ӧ3A��g��+B��g���TxC��g��+2D��g������5min���D��Ũ��Ϊ0.5mol?L-1��c��A����c��B��=3��5��C��ƽ����Ӧ������0.1mol/��L?min������
��1����ʱ��A�����ʵ���Ũ��Ϊ______��
��2����Ӧ��ʼǰ������A��B�����ʵ���Ϊ______��
��3��B��ƽ����Ӧ����Ϊ______��
��4��x��ֵΪ______��
5��ѡ���� ��ͬ�¶��£��������ȵĶ��������ܱ������з������淴Ӧ��
N2 ��g��+3H2��g�� 2NH3��g����H=" ��92.4" kJ/mol��
2NH3��g����H=" ��92.4" kJ/mol��
ʵ������ʼ��ƽ��ʱ���й��������±���
�������
| ��ʼʱ���������ʵ���/mol
| ��ƽ��ʱ��Ӧ�е������仯
|
N2
| H2
| NH3
|
��
| 1
| 3
| 0
| �ų�����a kJ
|
��
| 2
| 6
| 0
| �ų�����bkJ?
|
����������ȷ���ǣ�?��
A���ų�������ϵ��b��2a? B���ų�������ϵ��b =2a
C����ƽ��ʱ����������������٣���? D��N2��ת���ʣ��٣���