| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学知识点总结《物质组成与性质实验方案的设计》考点巩固(2019年最新版)(十)
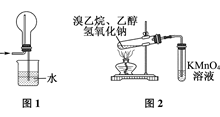 参考答案:C 本题解析:A错,浓硫酸不能氧化二氧化硫,可以干燥; 本题难度:一般 4、填空题 二氧化氯(ClO2)作为一种高效强氧化剂,已被联合国世界卫生组织(WHO)列为AI级安全消毒剂.常温下二氧化氯为黄绿色或橘黄色气体,性质非常不稳定.温度过高,二氧化氯的水溶液有可能爆炸.某研究小组设计如图所示实验制备ClO2. 参考答案:(1)KClO3和草酸(H2C2O4)在酸性条件下反应生成ClO2、CO2和KHSO4,反应的方程式为2KClO3+H2C2O4+2H2SO4?△?.?2ClO2↑+2CO2↑+2KHSO4+2H2O,氧化产物为CO2,还原产物为ClO2,二者物质的量之比为1:1, 本题解析: 本题难度:简单 5、填空题 实验室制取溴苯的装置示意图及有关数据如下:
(1)在a中加入15mL苯和少量铁屑.在b中小心加入4.0mL液态溴.向a中滴入液溴,至 液溴滴完. ①装置d中NaOH的作用是______; ②a的名称是______; ③该反应是否要加热______(填下列字母) A.直接加热B.水浴加热C.不需加热 (2)反应完后,经过下列步骤分离提纯: ①向a中加入10mL水,然后过滤除去未反应的铁屑; ②滤液依次用10mL水、8mL10%的NaOH溶液、10mL水洗涤.NaOH溶液洗涤的作用是______ ③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤.加入氯化钙的目的是______ (3)经以上分离操作后,粗溴苯中还含有的主要杂质为______,要进一步提纯,下列操作中必须的是______(填入正确选项前的字母); A.分液B.过滤C.萃取D.蒸馏 (4)在该实验中,a的容积最适合的是______(填入正确选项前的字母). A.25mLB.50mLC.250mLD.500mL. 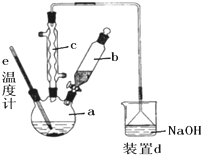 参考答案:(1)①液溴都易挥发,而苯的卤代反应是放热的,尾气中有HBr及挥发出的Br2,用氢氧化钠溶液吸收,防止污染大气,故答案为:吸收HBr和Br2; 本题解析: 本题难度:一般 |
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学知识点整理《电解质和非.. | |