1、选择题 下列各组混合物,可以用分液漏斗分离的是
A.甲苯和水
B.甲苯和苯
C.溴乙烷与水
D.苯与溴乙烷
参考答案:AC
本题解析:分液漏斗可以将互不相溶的两层液体分开。BD项:两种物质互溶,不能用分液漏斗分离,故错。故选AC。
点评:本题考查学生物质分离方法中的分液法,熟记教材知识是解题的关键所在,难度不大。
本题难度:简单
2、选择题 关于某无色溶液中所含离子的鉴别,下列判断正确的是
A.加入AgNO3溶液,生成白色沉淀,加稀盐酸沉淀不溶解,可确定有Cl―存在
B.加入几滴Fe2(SO4)3溶液,溶液变成紫色,可确定有酚羟基存在
C.加入Ba(NO3)2溶液,生成白色沉淀,加稀盐酸沉淀不消失,可确定有SO42-存在
D.加入盐酸,生成的气体能使澄清石灰水变浑浊,可确定有CO32-存在
参考答案:B
本题解析:A、加入AgNO3溶液,生成白色沉淀,溶液中可能含有碳酸根离子、硫酸根离子,也会产生白色沉淀,故A错误;B、铁离子能和酚羟基反应而使溶液显紫色,所以选项B正确;C、由于在酸性条件下NO3-具有强氧化性,如果溶液中含有SO32-,与Ba2+反应生成白色沉淀BaSO3,然后加入盐酸,NO3-将BaSO3沉淀氧化生成BaSO4,所以不能确定有SO42-存在,C不正确;D、某固体加入盐酸,生成的气体能使澄清石灰水变浑浊,可能生成的是二氧化硫气体,不能说明原固体是碳酸盐,也可能是碳酸氢盐或亚硫酸盐等,故D错误,答案选B。
本题难度:一般
3、选择题 为提纯下列物质(括号内物质为杂质),所选用的试剂和分离方法正确的是( )
| 物质 | 除杂试剂 | 分离方法
A
硝酸铜溶液(硝酸银)
铜粉
结晶
B
NaCl溶液(CuCl2)
NaOH溶液
萃取
C
乙醇(水)
________
分液
D
铜粉(铁粉)
稀盐酸
过滤
|
A.A
B.B
C.C
D.D
参考答案:D
本题解析:
本题难度:一般
4、选择题 下列除杂的方法正确的是(? )?
A.除去N2中的少量O2:通过灼热的CuO粉末,收集气体
B.除去CO2中的少量HCl:通入Na2CO3溶液,收集气体
C.除去NaCl溶液中少量CaCl2:加入适量Na2CO3,过滤
D.除去KCl溶液中少量MgCl2:加入适量NaOH溶液,过滤
参考答案:C
本题解析:A错,除去N2中的少量O2:通过灼热的Cu网,收集气体;B错,除去CO2中的少量HCl:通入饱和NaHCO3溶液,收集气体;C正确;D错,除去KCl溶液中少量MgCl2:加入适量KOH溶液,过滤
本题难度:简单
5、选择题 下列实验操作与预期实验目的或所得实验结论一致的是(?)
选项
| 实验操作和现象
| 预期实验目的或结论
|
A
| 用洁净的铂丝蘸取某食盐试样,在酒精灯火焰上灼烧,火焰显黄色
| 说明该食盐不是加碘盐
|
B
| 银氨溶液中滴入少量组成为C2H4O2的液态有机物,水浴微热,有银镜出现
| 可确定该有机物一定是甲酸甲酯
|
C
| 向两支盛有KI3的溶液的试管中,分别滴加淀粉溶液和AgNO3溶液,前者溶液变蓝,后者有黄色沉淀
| KI3溶液中存在平衡:I?I2
+I-
|
D
| 室温下向CuCl2和少量FeCl3的混合溶液中,加入铜屑,充分搅拌,过滤,得蓝绿色溶液
| 除去杂质FeCl3得纯净CuCl2
溶液
|
?
参考答案:C
本题解析:A项,钾的焰色反应应透过蓝色钴玻璃片观察,显紫色,错误;B项,也可以是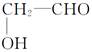 ,错误;C项I2使淀粉变蓝,I-和Ag+反应生成黄色沉淀;D项,加入铜屑发生2Fe3++Cu=2Fe2++Cu2+,不能除去生成的FeCl2。
,错误;C项I2使淀粉变蓝,I-和Ag+反应生成黄色沉淀;D项,加入铜屑发生2Fe3++Cu=2Fe2++Cu2+,不能除去生成的FeCl2。
本题难度:一般