1、选择题 在某无色溶液中缓慢地滴入NaOH溶液直至过量,产生沉淀的质量与加入的NaOH溶液体积的关系如下图所示,由此确定,原溶液中含有的阳离子是( )
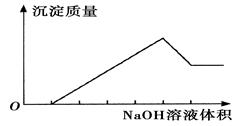
A.H+、Al3+、Fe2+
B.H+、Mg2+、Al3+
C.H+、Ba2+、Al3+
D.只有Mg2+、Al3+
参考答案:B
本题解析:第一阶段无沉淀,水溶液中一定含有氢离子,故AD错误,第三阶段有部分沉淀能和氢氧化钠继续反应,说明部分沉淀是氢氧化铝,原溶液中一定含有铝离子,第四阶段沉淀的量不再随着氢氧化钠量的增多而增加,说明一定有一种沉淀和氢氧化钠不反应,可推知该沉淀是氢氧化镁,原溶液中一定含有镁离子。
故选B。
点评:题考查金属镁以及金属铝的化合物的有关性质,注意氢氧化铝能和强碱反应是解题的关键所在,难度不大。
本题难度:简单
2、选择题 下列反应的离子方程式书写不正确的是( )
A.少量稀硫酸溶液加入氢氧化钡溶液中:Ba2++OH-+H++SO42-=BaSO4↓+H2O
B.向KAl(SO4)2溶液中逐滴加入Ba(OH)2溶液至SO42-完全沉淀:Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO2-+2H2O
C.碳酸氢钠溶液与少量硫酸氢钠溶液反应:HCO3-+H+=CO2↑+H2O
D.硫酸铝与足量氨水反应:Al3++3NH3?H2O=Al(OH)3↓+3NH4+
参考答案:A、少量稀硫酸溶液加入氢氧化钡溶液中后,硫酸全反应,氢离子和硫酸根按物质的量之比是2:1反应,即Ba2++2OH-+2H++SO42-=BaSO4↓+H2O,故A错误;
B、KAl(SO4)2溶液中逐滴加入Ba(OH)2溶液至SO42-完全沉淀时,发生的反应为:Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO2-+2H2O,故B正确;
C、碳酸氢钠溶液与少量硫酸氢钠溶液反应实质是碳酸氢根和氢离子之间的反应,即:HCO3-+H+=CO2↑+H2O,故C正确;
D、硫酸铝与足量氨水反应实质是氯离子和氨水之间反应生成沉淀的过程,即:Al3++3NH3?H2O=Al(OH)3↓+3NH4+,故D正确.
故选A.
本题解析:
本题难度:简单
3、选择题 下列反应的离子方程式正确的是( )
A.氯化钡溶液与硫酸反应:Ba2++SO
=BaSO4↓
B.金属镁与稀盐酸反应:Mg+2H++2Cl-=MgCl2+H2↑
C.碳酸钠溶液与盐酸反应:Na2CO3+2H+=2Na++H2O+CO2↑
D.氢氧化镁与硫酸溶液反应:OH-+H+=H2O
参考答案:A.氯化钡与硫酸反应生成了硫酸钡,反应的离子方程式为:SO42-+Ba2+=BaSO4↓,故A正确;
B.金属镁与稀盐酸反应的实质为镁与氢离子反应生成氢气和镁离子,正确的离子方程式为:Mg+2H+=Mg2++H2↑,故B错误;
C.碳酸钠不能保留化学式,正确的离子方程式为:CO32-+2H+=H2O+CO2↑,故C错误;
D.氢氧化镁为难溶物,应该两边化学式,正确的离子方程式为:Mg(OH)2+2H+=2H2O+Mg2+,故D错误;
故选A.
本题解析:
本题难度:一般
4、选择题 下列离子方程式不正确的是(?)
A.用稀硫酸除去铜绿:4H++Cu2(OH)2CO3=2Cu2++CO2↑+3H2O
B.将Na2O2固体投入H218O中:2H218O+2Na2O2=4OH-+4Na++18O2↑
C.向NH4Al(SO4)2溶液中滴入Ba(OH)2溶液恰好使SO42―完全沉淀:
2Ba2++NH4++Al3++2SO42―+4OH-= Al(OH)3↓+NH3・H2O+2BaSO4↓
D.向Na2FeO4溶液中加入稀硫酸产生氧气:4FeO42―+20H+ = 4Fe3++3O2↑+10H2O
参考答案:B
本题解析:A、符合反应规律和电荷守恒、原子守恒,正确;B、该反应氧化剂和还原剂都是Na2O2,O2中O元素来源于Na2O2,不是18O,错误;C、SO42―完全沉淀,则Ba2+和SO42?的系数相等,根据NH4Al(SO4)2和Ba(OH)2中各离子的比例,配平可得离子方程式,正确;D、FeO42―在酸性条件下发生氧化还原反应,生成Fe3+、O2、H2O。
本题难度:一般
5、选择题 下列反应的离子方程式中,正确的是
[? ]
A.稀硫酸滴在银片上:2Ag+2H+=2Ag++H2↑
B.稀硫酸与氢氧化钡溶液混合:SO42-+Ba2+=BaSO4↓
C.稀硝酸滴在大理石上:CaCO3+2H+=Ca2++H2CO3
D.氧化铁与稀盐酸混合:Fe2O3+6H+=2Fe3++3H2O
参考答案:D
本题解析:
本题难度:一般