1、选择题 下列各组元素性质递变情况表述错误的是
A.Li、Be、B原子最外层电子数逐渐增多
B.N、O、F原子半径依次增大
C.Li、Za、K、Rb的金属性依次增强
D.P、S、Cl最高正价依次升高
2、选择题 下列分子中σ键是以s轨道与sp2杂化轨道“头碰头”方式重叠而成的是
A.C2H2
B.HCl
C.H2O
D.C2H4
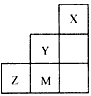
3、选择题 下图为元素周期表中短周期的一部分,关于推断Y、Z、M 的说法正确的是
[? ]
A.非金属性:Y>Z>M
B.离子半径:M- >Z2- >Y-
C.ZM2分子中各原子的最外层均满足8电子稳定结构
D.三种元素中,Y的最高价氧化物对应的水化物酸性最强
4、推断题 短周期主族元素A、B、C、D、E原子序数依次增大,A为周期表中半径最小的元素,B原子的最外层电子数是其电子层数的2倍,D、E同主族,E的原子序数是D的2倍。
(1)A、C元素可以形成多种化合物,其中甲是火箭推进剂中常用的液态燃料,甲中A、C元素的质量比为7:1。已知0.4mol液态甲和氧气完全反应生成氮气和液态水放出248.8kJ的热量,写出该反应的热化学方程式____________?。
(2)在直接以液态甲为燃料的电池中,电解质溶液为NaOH溶液,负极的反应式为___________,理想状态下,该燃料电池消耗1mol液态甲所能产生的最大电能为528.7kJ,则该燃料电池的理论效率为________(燃料电池的理论效率是指电池所产生的最大电能与燃料电池反应所能释放的全部能量之比)。
(3)A、B、D元素可以形成化合物乙,其化学式为A2B2D4,0.2mol/L的乙溶液和0.2mol/L的NaOH溶液等体积混合,所得溶液显酸性,则该溶液中各离子浓度由大到小排列的顺序为_______________?。
(4)将8mL?0.1mol/L的酸性高锰酸钾溶液和2mL?1.0mol/L的乙溶液在试管中混合,将试管置于25℃水中(如下图所示)。KMnO4浓度随时间变化关系如下图所示。

①写出发生反应的离子方程式_______________?;
②计算前40秒用乙表示的平均反应速率,v(乙)______________;
③40s~65s的反应速率比前40s快,解释原因_______________?。
5、选择题 下列各粒子半径依次增加的是( )
A.Cs+K+Mg2+Al3+
B.F? F-Cl-Br-
C.Ca2+K+S2-Cl-
D.Al? Al3+Mg? K