1、简答题 某同学帮助水质检测站配制960mL?1mol?L-1NaOH溶液以备使用.
(1)该同学应选择______mL的容量瓶.
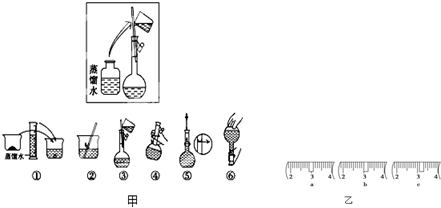
(2)其操作步骤如图甲所示,则如图操作应在图中的______(填选项字母)之间.
A.②与③B.①与②C.④与⑤
(3)该同学应称取NaOH固体______g,用质量为23.1g的烧杯放在托盘天平上称取所需NaOH固体时,请在附表中选取所需的砝码大小______(填字母),并在图乙中选出能正确表示游码位置的选项______(填字母).
附表 砝码规格
(4)下列操作对所配溶液的浓度大小有何影响?
①转移完溶液后未洗涤玻璃棒和烧杯,浓度会______(填“偏大”“偏小”或“无影响”,下同).
②容量瓶中原来有少量蒸馏水,浓度会______.
参考答案:(1)实验室没有960mL的容量瓶,性质大于960mL且规格相近的容量瓶,故应选1000mL容量瓶,故答案为:1000;
(2)如图所示的操作为移液洗涤后向容量瓶内加水,应在加水振荡与定容之间,即应在④与⑤之间,故选:C;
(3)配制1000mL1mol?L-1NaOH溶液需要氢氧化钠的质量为1L×1mol/L×40g/mol=40.0g;
氢氧化钠具有腐蚀性且易潮解,应放在烧杯内称量,根据氢氧化钠与烧杯总质量为40.0g+23.1g=63.1g,故应选择50g与10g的游码,即选择bd;
由表中升高可知,最小的砝码为5g,故游码的最大刻度为5g,故小于5g所以游码,所以游码应在3.1g的位置,故选择c,
故答案为:40.0;bd;c;
(4)①转移完溶液后未洗涤玻璃棒和烧杯,玻璃棒、烧杯壁上沾有少量的氢氧化钠,移入容量瓶内的氢氧化钠的质量减少,所配溶液的浓度偏小,
故答案为:偏小;
②溶液配制需加水定容,容量瓶中原来有少量蒸馏水,对所配溶液浓度无影响,故答案为:无影响.
本题解析:
本题难度:一般
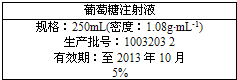
2、简答题 为维持人体血液中的血糖含量,在给病人输液时,通常用葡萄糖注射液,下图是医院给病人输液时使用的一瓶质量分数为5%的葡萄糖(C6H12O6)注射液的标签.某学生欲在实验室中配制500mL该葡萄糖注射液.
实验用品:葡萄糖固体、蒸馏水、烧杯、容量瓶(500mL)、药匙、胶头滴管、量筒.
(1)还缺少的仪器有______.
(2)下列对容量瓶及使用的描述中不正确的是______.
A.容量瓶上标有容积、温度和浓度
B.使用前要检查容量瓶是否漏水
C.容量瓶用蒸馏水洗净后,再用5%葡萄糖注射液洗
D.配制溶液时,把称好的葡萄糖晶体小心倒入容量瓶中,加入蒸馏水到接近刻度线1~2cm处,改用胶头滴管加蒸馏水至刻度线
(3)实验中需取用固体的质量为______g,该葡萄糖注射液的物质的量浓度______mol/L.
(4)配制该葡萄糖注射液,下列操作会导致所配溶液的物质的量浓度偏高的是______.
A.没有将洗涤液转移到容量瓶B.定容时俯视刻度线
C.容量瓶洗净后未干燥D.定容时液面超过了刻度线.
参考答案:(1)因配制步骤有:称量、溶解、移液、洗涤、定容、摇匀等操作,一般用托盘天平称量,用药匙取药品,放在小烧杯中称量,然后在烧杯中溶解(可用量筒量取水),冷却后转移到500ml容量瓶中,并用玻璃棒引流,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,盖好瓶塞颠倒反复摇匀,
所以需要的仪器为:托盘天平、烧杯、药匙、玻璃棒、500mL容量瓶、胶头滴管,
故答案为:托盘天平、玻璃棒;
(2)A.容量瓶上标明容积、温度和刻度线,故A错误;
B.配制最后需颠倒,上下反复摇匀,使用前要检查容量瓶是否漏水,故B正确;
C.用标准葡萄糖注射液润洗,容量瓶内壁沾有少量葡萄糖,所配葡萄糖溶液的浓度偏高,故C错误;
D.物质溶解或稀释会生成热效应,对溶液体积有影响,甚至使容量瓶受热不均导致破裂的危险,容量瓶不能直接用来溶解固体,故D错误;
故答案为:ACD;
(3)葡萄糖(C6H12O6)注射液的密度为1.08g?mL-1,500mL溶液,葡萄糖的质量分数5%,则含葡萄糖的质量为:500mL×1.08g/cm3×5%=27.0g,葡萄糖的物质的量为27g180g/mol=0.15mol,溶质的物质的量浓度为0.15mol0.5L=0.3mol/L,故答案为:27.0;0.3;
(4)A.没有将洗涤液转移到容量瓶,移入容量瓶内溶质的物质的量减小,所配溶液的浓度偏低,故A不符合;
容量瓶中原有少量蒸馏水,故A错误;
B.定容时俯视刻度线,液面再刻度线下方,所配溶液的体积偏小,所配溶液的浓度偏高,故B符合;
C.配制需加水定容,容量瓶洗净后未干燥,对体积和物质的量均无影响,对所配溶液浓度无影响,故C不符合;
D.定容时液面超过了刻度线,溶液的体积偏大,所配溶液的浓度偏低,故D不符合;
故答案为:B.
本题解析:
本题难度:一般
3、选择题 NA表示阿伏伽德罗常数,下列判断正确的是( )
A.在18 g18O2中含有NA个氧原子
B.标准状况下,22.4L空气含有NA个单质分子
C.1 mol Cl2参加反应转移电子数一定为2 NA
D.含NA个Na+ 的Na2O溶解于1L水中,Na+ 的物质的量浓度为1mol・L―1
参考答案:A
本题解析:A、18g18O2物质的量是0.5mol,一个氧气分子含有两个氧原子,所以氧原子物质的量为1mol,即1NA,正确;B、空气是混合物,标准状况下,22.4L空气是1mol,但空气中含有氧气、氮气、二氧化碳、稀有气体等,共计1mol,单质的物质的量小于1mol,错误;C、1molCl2参加反应,如果只做氧化剂则转移电子数2mol,若自身氧化还原反应,则转移电子数为1mol,错误;D、含NA个Na+的Na2O溶解于1L水中,可得氢氧化钠为1mol,但Na2O与H2O反应,溶液的体积不是1L,所以物质的量浓度不是1mol/L,错误。
本题难度:一般
4、选择题 0.012kg14C含有的碳原子数?
[? ]
A.等于NA?
B.小于NA
C.大于NA
D.无法判断
参考答案:B
本题解析:
本题难度:简单
5、选择题 下列溶液中,Na+数目最多的是( )
A.1mol/L?Na2SO4溶液200mL
B.0.9mol/L?Na3PO4溶液200mL
C.2.5mol/L?NaOH?溶液100mL
D.1mol/L?NaHCO3溶液300mL
参考答案:B
本题解析:
本题难度:简单