1、选择题 向某无色溶液中加入BaCl2溶液,生成不溶于稀硝酸的白色沉淀,则溶液中含有的离子是
A.一定有 CO32-
B.一定有Ag+
C.一定有SO42-
D.无法确定
2、选择题 用下图所示方法,检验某固体中是否含有Cl―,下列说法正确的是

A.①是BaCl2溶液,②稀盐酸
B.①是稀盐酸,②稀BaCl2溶液
C.①是稀硝酸,②是AgNO3溶液
D.①是稀硫酸,②是AgNO3溶液
3、选择题 由H79Br和H81Br组成的混合气体对N2的相对密度为2.9,则气体中79Br和81Br的原子个数比为
A.1:1
B.1:2
C.2:3
D.3:2
4、选择题 在pH为4-5的环境中,Cu2+、Fe2+不生成沉淀,而Fe3+几乎完全沉淀。工业上制CuCl2是将浓盐酸用蒸汽加热到80℃ 左右,再慢慢加入粗氧化铜(含杂质FeO),充分搅拌使之溶解。欲除去溶液中的杂质离子,下述方法中可行的是
[? ]
A.加入纯Cu将Fe2+还原
B.在溶液中通入Cl2,再加入CuO粉末调节pH为4~5
C.向溶液中通入H2S使Fe2+沉淀
D.在溶液中通入Cl2,再通入NH3调节pH为4-5
5、填空题 为回收利用废钒催化剂(含有V2O5、VOSO4及不溶性残渣),科研人员最新研制了一种离子交换法回收钒的新工艺,主要流程如下:
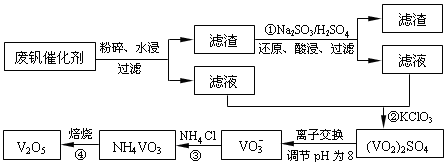
部分含钒物质在水中的溶解性如下:
物质
| VOSO4
| V2O5
| NH4VO3
| (VO2)2SO4
|
溶解性
| 可溶
| 难溶
| 难溶
| 易溶
|
?
回答下列问题:
(1)工业由V2O5冶炼金属钒常用铝热剂法,该反应的氧化剂为_____________。
(2)滤液中含钒的主要成分为______________(填化学式)。
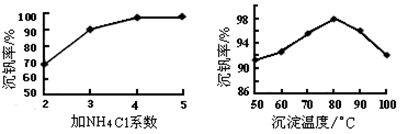
(3)该工艺中反应③的沉淀率(又称沉钒率)是回收钒的关键之一,该步反应的离子方程式____;沉钒率的高低除受溶液pH影响外,还需要控制氯化铵系数(NH4Cl加入质量与料液中V2O5的质量比)和温度。根据下图判断最佳控制氯化铵系数和温度为___________、_________℃。
(4)用硫酸酸化的H2C2O4溶液滴定(VO2)2SO4溶液,以测定反应②后溶液中含钒量,反应方程式为:2VO2++H2C2O4+2H+=2VOn+ + 2CO2↑+ mH2O,其中n、m分别为______________、________ 。
(5)全钒液流电池的电解质溶液为VOSO4溶液,电池的工作原理为: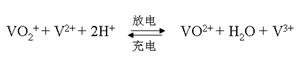
电池放电时正极的电极反应式为?。