1、选择题 下列说法中正确的是( )
A.氧的摩尔质量为32
B.阿伏加德罗常数是6.02×1023
C.某硫酸溶液中H2SO4的质量分数为60%
D.1摩尔硫酸在标准状况下的体积是22.4升
参考答案:A、氧气的摩尔质量为32g/mol,故A错误;
B、阿伏加德罗常数是6.02×1023/mol,故B错误;
C、溶质质量分数是溶质质量占溶液质量的百分比,故C正确;
D、硫酸不是气体,故D错误;
故选C.
本题解析:
本题难度:简单
2、选择题 下列说法不正确的是(NA表示阿伏加德罗常数的值)( )
A.28g氮气所含有的原子数目为2NA
B.4g金属钙变成钙离子时失去的电子数目为0.1NA
C.1mol甲烷的质量与NA个甲烷分子的质量之和相等
D.标准状况下,22.4L甲烷和乙烯混合物所含的分子数为NA
参考答案:A、N(N)=2N(N2)=2n(N2)NA=2m(N2)M(N2)NA=228g28g/molNA=2NA,故A正确;
B、40g金属钙变成钙离子时失去的电子数目为2NA,所以4g金属钙变成钙离子时失去的电子数目为0.2NA,故B错误;
C、NA个甲烷分子的物质的量为1mol,所以1mol甲烷的质量与NA个甲烷分子的质量相等,故C正确;
D、标况下,22.4L任何气体的物质的量都是1mol,所以22.4L甲烷和乙烯混合物的物质的量为1mol,N=nNA=1mol×NA=NA,所以22.4L甲烷和乙烯混合物所含的分子数为NA,故D正确;
故选B.
本题解析:
本题难度:一般
3、选择题 设NA为阿伏加德罗常数的值。下列叙述正确的是
[? ]
A.常温常压下,22.4 L氯气与足量NaOH溶液反应转移电子数为NA
B.在含有NA个醋酸根离子(CH3COO-)的醋酸溶液中氢离子数目为NA
C.4.6 g SO2、CO2混合气体中含有中子数为2.3NA
D.1 mol CnH2n+2分子中含共价键数目为(3n+2)NA
参考答案:C
本题解析:
本题难度:简单
4、选择题 用NA表示阿伏加德罗常数的值,下列说法正确的是( )
A.lmolN2O2与水完全反应时转移电子的数目为NA
B.标准状况下,22.4L水中含有水分子的数目为NA
C.将0.1molFeCl3水解制成胶体,所得胶体粒子数为0.1NA
D.1L0.1mol?L-1乙酸溶液中H+数为0.1NA
参考答案:A、过氧化钠与水反应,过氧化钠起氧化剂与还原剂作用,各占12,lmolN2O2与水完全反应时转移电子的数目为0.5mol×2×NAmol-1=NA,故A正确;
B、标准状况下,水是液体,不能使用气体摩尔体积,故B错误;
C、Fe(OH)3胶体胶粒是很多Fe(OH)3的集合体,且氯化铁不能完全水解,所得胶体粒子数小于0.1NA,故C错误;
D、乙酸是弱电解质,电离程度不大,溶液中氢离子浓度远小于0.1mol/L,所以1L该溶液中H+数远小于1L×0.1mol/L×NAmol-1=0.1NA,故D错误.
故选A.
本题解析:
本题难度:简单
5、选择题 NA表示阿伏加德罗常数的值,下列说法正确的是
A.常温常压下,1mol 氦气含有2NA个核外电子
B.常温常压下,当活泼金属转移2NA个电子时,可从盐酸中置换出22.4L H2
C.标准状况下,0.5NA个CCl4所占的体积约为11.2L
D.42g NaHCO3固体含有的离子数为1.5NA
参考答案:A
本题解析:分析:A、氦气是单原子分子,每个氦原子有2个电子,根据N=nNA计算电子数目.
B、活泼金属转移2NA个电子,可以从盐酸中置换出1mol H2,常温常压下,气体摩尔体积大于22.4L/mol.
C、标准状况下,四氯化碳是液体,不能使用气体摩尔体积.
D、根据n=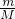 计算碳酸氢钠的物质的量,碳酸氢钠是离子化合物,由钠离子与碳酸氢根离子构成.
计算碳酸氢钠的物质的量,碳酸氢钠是离子化合物,由钠离子与碳酸氢根离子构成.
解答:A、氦气是单原子分子,每个氦原子有2个电子,所以1mol 氦气含有2NA个核外电子,故A正确;
B、活泼金属转移2NA个电子,可以从盐酸中置换出1mol H2,常温常压下,气体摩尔体积大于22.4L/mol,所以氢气体积大于22.4L,故B错误;
C、标准状况下,四氯化碳是液体,不能使用气体摩尔体积,故C错误;
D、42g NaHCO3固体的物质的量为0.5mol,碳酸氢钠由钠离子与碳酸氢根离子构成,离子物质的量为1mol,所以含有的离子数为NA,故D错误.
故选:A.
点评:考查常用化学计量有关计算,难度不大,注意气体摩尔体积的使用条件与对象,可借助pV=nRT理解气体摩尔体积数值.
本题难度:一般