1、选择题 已知1.505×1023个X气体分子的质量为16g,则X气体的摩尔质量是?
A.32 g
B.64 g
C.64 g/rnol
D.32 g/mol
参考答案:C
本题解析:略
本题难度:简单
2、选择题 从下列事实所得出的结论或给出的解释正确的是( )
| 实验事实 | 结论或解释
①
将40g?NaOH溶于1L蒸馏水中
该溶液中溶质的质量分数为3.84%,其物质的量浓度为1mol?L-1
②
向盛有1mL?0.1mol?L-1AgNO3溶液的试管中滴加0.1mol?L-1NaCl溶液,至不再有沉淀生成,再向其中滴加?0.1mol?L-1KI溶液,白色沉淀转化为黄色沉淀.
常温下,S(AgCl)<S(AgI)
③
Mg(OH)2难溶于水但可溶于NH4Cl溶液
NH4Cl水解显酸性,Mg(OH)2与H+发生反应
④
某盐NaX溶液pH>7
酸HX为弱酸
⑤
向某溶液中加入2滴KSCN溶液,溶液不显红色;再向溶液中加入几滴新制的氯水,溶液变为红色
说明溶液中一定含有Fe2+
⑥
向盛有浓硝酸的试管中分别加入Al片和Cu片,前者没有明显现象,后者反应剧烈,产生大量红棕色气体
还原性Al<Cu
⑦
BaSO4的水溶液导电性很差
BaSO4是弱电解质
|
A.①⑤⑥
B.④⑤
C.③④⑥⑦
D.③④⑤⑦
参考答案:①水的密度为1g/ml,将40g?NaOH溶于1L蒸馏水中,溶液质量为1040g,质量分数为40g1040g×100%=3.85%;
40g氢氧化钠的物质的量为1mol,溶于水配成1L溶液,溶液浓度为1mol/L,溶液体积为1L,能使溶剂体积.故①错误;
②向盛有1mL?0.1mol?L-1AgNO3溶液的试管中滴加0.1mol?L-1NaCl溶液,至不再有沉淀生成,再向其中滴加?0.1mol?L-1KI溶液,白色沉淀转化为黄色沉淀.说明相同体积的溶液中溶解的氯化银的物质的量多,溶解碘化银的物质的量少,即Ksp(AgCl)<Ksp(AgI).故②错误;
③Mg(OH)2电离出来的OH-与NH4+结合生成难电离的弱电解质NH3?H2O,从而使Mg(OH)2的溶解平衡向右移动,故
Mg(OH)2能溶于NH4Cl溶液中,水解形成的H+的浓度很小,不是Mg(OH)2溶解的主要因素.故③错误;
④某盐NaX溶液pH>7,钠离子为强碱离子,不能水解,说明X-离子发生水解,破坏水的电离平衡,HX为弱酸,故④正确;
⑤铁离子遇KSCN溶液,溶液显红色,开始加入2滴KSCN溶液,溶液不显红色;再向溶液中加入几滴新制的氯水,溶液变为红色,说明加入氯水后有铁离子生成,则原溶液中含有亚铁离子,故⑤正确;
⑥还原性铝强于铜,铝在浓硝酸中发生钝化,生成一层致密的氧化物保护膜,阻止进一步反应,故⑥错误;
⑦溶液导电性与离子浓度及离子所带电荷有关,与强弱电解质无关,硫酸钡是强电解质,溶解度很小,离子浓度很小,导致溶液导电性很差,故⑦错误.
故④⑤正确.
故选:B.
本题解析:
本题难度:简单
3、选择题 20 g氢氧化钠固体溶于水,配制500mL溶液,该溶液的物质的量浓度为
[? ]
A、1.0mol/L
B、0.5mol/L
C、20mol/L
D、0.04mol/L
参考答案:A
本题解析:
本题难度:简单
4、选择题 在容积为1L的干燥烧瓶中,用向下排空气法充入NH3后,测得烧瓶中的气体对氢气的相对密度为9.7。若将此气体进行喷泉实验,当喷泉停止后进入烧瓶中溶液的体积应为
A. L
L
B.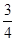 L
L
C.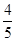 L
L
D. L
L
参考答案:C
本题解析:气体密度比等于相对分子质量比,所以烧瓶中气体平均相对分子质量为19.4。用排空气法收集氨气,氨气不纯,其中混有空气,由十字交叉法: 得氨气和空气体积比为4:1,所以进入烧瓶中溶液的体积为4/5L。
得氨气和空气体积比为4:1,所以进入烧瓶中溶液的体积为4/5L。
点评:掌握十字交叉法的运用。
本题难度:一般
5、计算题 (6分)取22.1g碳酸钠和碳酸氢钠的混合粉末样品,将其分成两等份,取其中一份加热到质量不再改变,冷却后称其质量为7.95g;另一份溶于水,配成600mL溶液。试计算(计算结果用小数形式表示):
(1)原样品中碳酸钠的物质的量为多少?
(2)所配溶液中Na+的物质的量浓度为多少?
参考答案:(6分)解:(1) 2NaHCO3 Na2CO3+CO2↑+H2O ............................(1分)
Na2CO3+CO2↑+H2O ............................(1分)
2mol? 44g+18g=62g
n( NaHCO3)? 11.05g-7.95g=3.1g
n( NaHCO3)=0.1mol
∴原样品中m(NaHCO3)="0.2mol×84g/mol=16.8g" .....................(1分)
m(Na2CO3)=22.1g-16.8g=5.3g
n(Na2CO3)= 0.05mol………………….(1分)
(2)由(1)可知一份中n( NaHCO3)="0.1mol?" n(Na2CO3)= 0.025mol
∴n(Na+)="0.1mol+0.025mol×2=0.15mol..................." (1分)
∴c(Na+)= ="0.25" mol・L-1......................(2分)
="0.25" mol・L-1......................(2分)
本题解析:略
本题难度:简单