|
|
|
高中化学知识点讲解《物质的量》在线测试(2019年最新版)(七)
2020-07-08 00:32:13
【 大 中 小】
|
1、选择题 设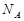 表示阿伏加德罗常数,下列说法正确的是 表示阿伏加德罗常数,下列说法正确的是
A.23 g钠与足量氧气充分反应,转移的电子个数为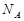
B.1mol Cl2与水充分反应,转移的电子个数为
C.1mol Na2O2与水完全反应时转移电子数为2NA
D.18 g H2O含有的电子数为18NA
2、选择题 下列说法正确的是
A.35Cl原子所含质子数为18
B.0.1 mol HCl所含分子数约为6.02×1022
C.3.5 g的35Cl2气体的体积为2.24 L
D.2 mol 35Cl2气体的质量为140 g
|
3、选择题 标准状况下将VL氨气溶解在1L水中(水的密度近似为1g/ml),所得溶液的密度为ρ g/mL,质量分数为w,物质浓度为c mol/L,则下列关系中不正确的是
A.ρ="(17V+22400)" /(22.4+22.4V)
B.w="17c/(1000ρ)"
C.w="17V/(17V+22400)"
D.C=1000Vρ/(17V+22400)
|
4、选择题 下列说法中不正确的是(?)
A.在同温同压下,1摩尔固体或液体的体积各不相同
B.在同温同压下,不同气体的摩尔体积都大致相同
C.气体摩尔体积约为22.4 L/ mol
D.只有在标准状况下,气体摩尔体积才约为22.4 L/ mol
5、填空题 绿矾(FeSO4・7H2O)在化学合成上用作还原剂及催化剂,工业上常用废铁屑溶于一定浓度的硫酸溶液制备绿矾。
(1)98% 1.84 g/cm3的浓硫酸在稀释过程中,密度下降,当稀释至50%时,密度为1.4g/cm3,50%的硫酸物质的量浓度为?(保留两位小数),50%的硫酸与30%的硫酸等体积混合,混合酸的浓度为?(填>、<、=)40%。
(2)实际生产用20%发烟硫酸(100克发烟硫酸含SO3 20克)配制稀硫酸,若用SO3・nH2O表示20%的发烟硫酸,则n=____________(保留两位小数)。
(3)绿矾在空气中容易被部分氧化为硫酸铁,现取7.32克晶体溶于稀盐酸后,加入足量的BaCl2溶液,过滤得沉淀9.32克;再通入112mL(标准状况)氯气恰好将Fe2+完全氧化,推测晶体的化学式为?。?
(4)硫酸亚铁铵[(NH4)2SO4・FeSO4・6H2O](俗称莫尔盐),较绿矾稳定,在分析化学中常用来配制Fe2+的标准溶液,用此Fe2+的标准溶液可以测定剩余稀硝酸的量。现取8.64克Cu2S和CuS的混合物用200mL2mol/L稀硝酸溶液处理,发生反应如下:
10NO3-+3Cu2S+16H+→6Cu2++10NO↑+3SO42-+8H2O
8NO3-+3CuS+8H+→ 3Cu2++3 SO42-+8NO↑+ 4H2O
剩余的稀硝酸恰好与V mL 2 mol/L (NH4)2Fe(SO4)2溶液完全反应。
已知:NO3-+3Fe2++4H+→ NO↑+3Fe3++2H2O
① V值范围?;
② 若V=48,试计算混合物中CuS的质量分数(保留两位小数)。