1、选择题 下列说法正确的是( )
A.需要加热才能发生的反应一定是吸热反应
B.化学反应中的能量变化都表现为热量变化
C.任何放热反应在常温下一定能发生反应
D.反应物和生成物所具有的总能量决定了反应是放热还是吸热
参考答案:A、放热反应有些也需要加热才能反应,可燃气体点燃反应,故A错误;
B、化学反应的能量变化除了热量外,还有光能等形式的能量转化,如镁条燃烧放热发光,故B错误;
C、有些放热反应必须加热才能反应,常温下不反应,故C错误;
D、反应物和生成物所具有的总能量决定了反应是放热还是吸热,若反应物总能量大于生成物总能量,则反应是放热反应,反之为吸热反应,故D正确;
故选D.
本题解析:
本题难度:简单
2、选择题 用如图所示装置(夹持仪器已略去)探究铜丝与过量浓硫酸的反应.下列实验不合理的是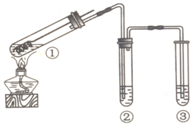
A.上下移动①中铜丝可控制SO2的量
B.为确认CuSO4生成,向①中加水,观察颜色
C.②中选用品红溶液验证SO2的生成
D.③中选用NaOH溶液吸收多余的SO2
参考答案:B
本题解析:分析:A.当铜丝与浓硫酸接触时才能反应;
B.根据溶液颜色的变化判断是否有CuSO4生成;
C.根据SO2的漂白性分析;
D.SO2为酸性气体,可与碱发生反应,
解答:A.当铜丝与浓硫酸接触时才能反应,当往上抽动铜丝时,铜丝与硫酸不接触,反应停止,故可通过上下移动①中铜丝可控制SO2的量,故A正确;
B.CuSO4溶液呈蓝色,可依据溶液颜色的变化判断是否有CuSO4生成,故B错误;
C.SO2具有漂白性,可用品红溶液验证SO2的生成,故C正确;
D.SO2为酸性气体,具有污染性,可与碱发生反应,用NaOH溶液吸收多余的SO2,故D正确.
故选B.
点评:本题考查二氧化硫的制备和性质,题目难度不大,注意A项,为制备二氧化硫的简易控制实验方法.
本题难度:一般
3、填空题 指出下列变化能量是怎样转化的:
(1)学校燃烧煤煮饭______(2)给手机的电池充电______
(3)用蓄电池点亮灯泡______.
参考答案:(1)学校燃烧煤煮饭将化学能转化为热能,故答案为:化学能转化为热能;
(2)给手机的电池充电将电能转化为化学能,故答案为:电能转化为化学能;
(3)用蓄电池点亮灯泡将化学能转化为电能,故答案为:化学能转化为电能.
本题解析:
本题难度:一般
4、选择题 下列有关化学反应能量变化的叙述一定正确的是
A.生成物总能量大于反应物总能量,该反应为放热反应
B.一个化学反应需要加热才能进行,该反应为吸热反应
C.应用盖斯定律,可计算某些难以直接测量的化学反应焓变
D.同温同压下,H2(g)+Cl2(g)===2HCl(g)在光照和点燃条件的?H不同
参考答案:C
本题解析:A.生成物总能量大于反应物总能量,该反应为吸热反应,故错误;B.一个化学反应需要加热才能进行,该反应不一定为吸热反应,错误;D.反应热?H只与反应的起始态和终态有关与反应的途径无关,应该是相同的,故错误;
本题难度:一般
5、选择题 X、Y、Z是三种气态物质,在一定温度下其变化符合下图.下列说法一定正确的是( )
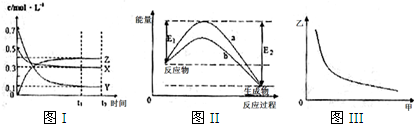
A.该反应热化学方程式为X(g)+3Y(g)?2Z(g)△H=-(E2-E1)
B.若图Ⅲ中甲表示压强,乙表示Z的含量,则其变化符合图Ⅲ中曲线
C.该温度下,反应的平衡常数数值约为533.若升高温度,该反应的平衡常数减小,Y的转化率降低
D.图Ⅱ中曲线b是加入催化剂时的能量变化曲线,曲线a是没有加入催化剂时的能量变化曲线
参考答案:A.图Ⅰ中X、Y的物质的量浓度逐渐减小,应是反应物,Z的物质的量浓度逐渐增大,应是生成物,浓度的变化比值为(0.5-0.3):(0.7-0.1):(0.4-0)=1:3:2,根据浓度的变化之比等于化学计量数之比可知反应方程式应为X(g)+3Y(g)

2Z(g),由图Ⅱ可知反应物的总能量大于生成物的总能量,反应放热,
反应热为△H=-(E2-E1)kJ/mol,该反应热化学方程式为X(g)+3Y(g)

2Z(g)△H=-(E2-E1)kJ/mol,反应热的单位为kJ/mol,故A错误;
B.压强增大,平衡右移,Z的含量应增大,故B错误;
C.该反应放热,升高温度平衡左移,该反应的平衡常数减小,Y的转化率降低,故C正确;
D.图Ⅱ也可能为加入不同的催化剂,b的催化效果较好,或是曲线b是加入催化剂,曲线a是没有加入催化剂时的能量变化曲线,故D错误.
故选C.
本题解析:
本题难度:一般