1��ѡ���� ���й��ڷ�Ӧ������˵����ȷ����
A��Zn��s��+CuSO4��aq����ZnSO4(aq)+Cu(s)��H=" -216" KJ/mol����Ӧ��������С��������������
B����ͬ�����£����1mol��ԭ�������е�����ΪE1��1mol����������е�����ΪE2����2E2=E1
C��101KPaʱ��2H2(g)��O2(g) ��2H2O(l) ��H=" -517.6" KJ/mol����������̬ˮ����HС��-517.6 KJ/mol
D������̫���ܵ������Դ���滯ʯȼ�ϣ������ڽ�Լ��Դ����������
�ο��𰸣�D
���������A����Ӧ���ȣ�˵����Ӧ��������������������������A����
B��1mol����Ӻ���2mol��ԭ�ӣ�������е�����Ϊ2mol��ԭ�ӵ���������E2=2E1��B����
C.Һ̬ˮת��Ϊ��̬ˮҪ���ȣ���������̬ˮ�ų�������Ҫ�٣�����HҪ��C����
D������̫���ܵ������Դ���滯ʯȼ�ϣ����ڽ�Լ��Դ��������������ȷ��
��ѡD
�����Ѷȣ�һ��
2��ѡ���� ��֪̼��һ����̼��������ȼ���ȷֱ��ǡ�H =-393��5kJ/mol����H ="-283" kJ/mol�͡�H ="-989" kJ/mol����ҵұ������跴Ӧ2C(s)+SiO2(s)=" Si" (s)+2 CO(g) ��H =
A��+768 kJ/mol
B��-768 kJ/mol
C��+2342 kJ/mol
D��-2342 kJ/mol
�ο��𰸣�A
�������������̼��һ����̼��������ȼ���ȷֱ��ǡ�H =-393��5kJ/mol����H ="-283" kJ/mol�͡�H ="-989" kJ/mol���ɷֱ�õ��Ȼ�ѧ����ʽ����C(s)+O2(g)=CO2(g) ��H =-393��5kJ?mol?1, ��CO(g)+1/2O2(g)=CO2(g) ��H ="-283" kJ?mol?1����Si(s)+ +O2(g)=SiO2(g) ��H ="-989" kJ/mol�����ݸ������ɣ���Ӧ2C(s)+SiO2(s)=" Si" (s)+2 CO(g)��Ч�ڢ١�2���ڡ�2���ۣ����ԡ�H =-393��5kJ/mol��2+283 kJ/mol��2+989 kJ/mol="+768" kJ/mol����A����ȷ��
�����Ѷȣ�һ��
3��ѡ���� ��֪����1mol?H2�����л�ѧ������ʱ��Ҫ����436kJ������
��1mol?Cl2�����л�ѧ������ʱ��Ҫ����243kJ������
����Hԭ�Ӻ�Clԭ���γ�1mol?HCl����ʱ�ͷ�431kJ������
����������ȷ���ǣ�������
A��������������Ӧ�����Ȼ���������Ȼ�ѧ����ʽ��H2��g��+Cl2��g��=2HCl��g��
B��������������Ӧ����2mol�Ȼ������壬��Ӧ�ġ�H=183kJ/mol
C��������������Ӧ����2mol�Ȼ������壬��Ӧ�ġ�H=-183kJ/mol
D��������������Ӧ����1mol�Ȼ������壬��Ӧ�ġ�H=-183kJ/mol
�ο��𰸣�A���Ȼ�ѧ����ʽӦ�����Ӧ�ȵ���ֵ����A����
B��H2��g��+Cl2��g��=2HCl��g���ķ�Ӧ��=������ļ��ܼ���Ӧ��ļ���=436kJ?mol-1+243kJ?mol-1-2��431?kJ?mol-1=-183kJ?mol-1����1mol������1mol������Ӧʱ�ų�����Ϊ183KJ����H=-183kJ/mol����B����
C����Ӧ��=������ļ��ܼ���Ӧ��ļ���=436kJ?mol-1+243kJ?mol-1-2��431?kJ?mol-1=-183kJ?mol-1����1mol������1mol������Ӧʱ�ų�����Ϊ183KJ����H=-183kJ/mol����C��ȷ��
D��������1mol�Ȼ�������ʱ���ų���������ԭ����һ�룬��H=-91.5kJ/mol����D����
��ѡC��
���������
�����Ѷȣ���
4��ѡ���� ����˵����ȷ����
A��H2��g����ȼ���ȡ�H����285.8 kJ/mol����2H2O��g����2H2��g����O2��g����H����571.6 kJ/mol
B����Ӧ��������������������������ʱ���÷�ӦΪ���ȷ�Ӧ
C����ʯī�Ƚ��ʯ�ȶ���֪��c�����ʯ��s����c��ʯī��s����H��0
D����֪��298Kʱ��N2��g����3H2��g�� 2NH3��g����H����92.0 kJ/mol������ͬ�¶��£����ܱ�������ͨ��1/2 mol N2��3/2 mol H2���ﵽƽ��ʱ�ų�46.0 kJ������
2NH3��g����H����92.0 kJ/mol������ͬ�¶��£����ܱ�������ͨ��1/2 mol N2��3/2 mol H2���ﵽƽ��ʱ�ų�46.0 kJ������
�ο��𰸣�C
���������ȼ��������һ�������£�1mol��ȼ����ȫȼ�������ȶ���������ʱ���ų����������������ȶ���������Һ̬ˮ��A����ȷ����Ӧ��������������������������ʱ���÷�ӦΪ���ȷ�Ӧ����֮�Ƿ��ȷ�Ӧ��B����ȷ������Խ�ͣ�Խ�ȶ����ɴ�ʯī���������ڽ��ʯ�ģ����Խ��ʯ����ʯī�ķ�Ӧ�Ƿ��ȷ�Ӧ��C��ȷ�������ĺϳ��ǿ��淴Ӧ��1/2 mol N2��3/2 mol H2����������1mol���������Էų�����������46.0 kJ��D����ȷ����ѡC��
�����Ѷȣ�һ��
5������� �����к��ȵIJⶨʵ����ա�
ȡ0.55 mol/L��NaOH��Һ50mL��0.5mol/L������50mL����ͼ3-4��ʾ��װ����
���з�Ӧ�Ͳⶨ�кͷ�Ӧ�ķ�Ӧ�ȡ�
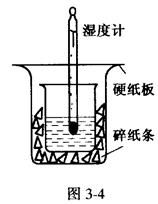
��1��ͼ3-4װ��ȱ�ٵ�һ��������____________��װ���л����ڵĴ�����____________�����ִ�����������¶ȶ���____________�����������С������Ӱ�족����
��2�����ձ�����������Ӳֽ�壬��õ��к��ȵ���ֵ��____________���ƫ����ƫС������Ӱ�족����
��3���ٶ�0.5mol/L�������0.55mol/L��NaOH��Һ���ܶȶ���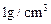 ���кͺ�������Һ�ı�����ΪC J/��g.�棩��Ӧǰ���¶�Ϊ18�棬��Ӧ������¶�Ϊt�棬���к��ȵļ���ʽ�ǡ�H=________________________��
���кͺ�������Һ�ı�����ΪC J/��g.�棩��Ӧǰ���¶�Ϊ18�棬��Ӧ������¶�Ϊt�棬���к��ȵļ���ʽ�ǡ�H=________________________��
��4��ʵ���У�������60mL 0.5mol/L���������ʵ�飬������ʵ������ȣ���ų�������____________������ࡱ������С������ȡ�������õ��к���____________
�����ͬ������ͬ������
�ο��𰸣���1��?���β��������?��С�ձ���û����ƽ��??��С??��
��2����С ?
��3��--4C��t-18��KJ�Mmol
��4��?����??����ͬ
�����������
�����Ѷȣ���