1������� ��������ҵ���������ɡ���������ȡ������ұ�������ļӹ��Ȼ��ڹ��ɡ���ش��������⣺
��1����ҵ�ϲ��õ���������ͱ���ʯ(Na3AlF6)������ķ���ұ���õ���������
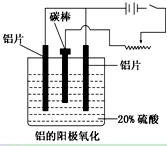
2Al2O3? ?4Al��3O2��
?4Al��3O2��
�������ʯ�����ã�________________________________________________��
��2��������������������������������Fe��Si�����ʣ����õ�ⷽ����һ���ᴿ���õ����������ĵ缫��ӦʽΪ________________�����п����������ϵ���__________��
A������?B��ʯī? C��Ǧ��?D������
��3������������ʹ���������������ܵ�����Ĥ����ϡ����Ϊ���Һ�������������ĵ缫��ӦʽΪ_____________________________________________________________��
��4�������������������У���Ҫ���ϵص�����ѹ��������_________________��
��5������˵����ȷ����__________________��
A������������Ӧ��ԭ���ԭ�����н������ϱ��洦���ļ���
B������������������ǿ������ľ�Ե����
C������������������߽���������Ͻ����ʴ�ԣ�����ĥ���½�
D��������������Ĥ���ж���ԣ����к�ǿ���������ܣ�������Ⱦ�϶��ʸ�����ɫ
2��ѡ���� ��ָ���������缫�����һ��Ũ�ȵ���Һ�ף�Ȼ�������������ʹ��Һ�ָ�Ϊ����Һԭ����Ũ�ȣ�����ʵ����ǣ�
?
| ����
| ����
| ��Һ��
| ������
|
A��
| Pt
| Pt
| NaOH
| NaOH����
|
B��
| Pt
| Pt
| H2SO4
| H2O
|
C��
| C
| Fe
| NaCl
| ����
|
D��
| ��ͭ
| ��ͭ
| CuSO4
| Cu(OH)2
3��ѡ���� ��ͼ��ʾ�����δ���Ʊ���ʳ��ˮ����������Mg2+������̼������Ƭ��������������ɣ�һ��ʱ�����Ƭ�������ֻ�����������������ȷ����
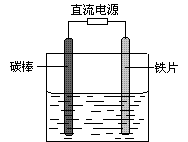
A��̼����ֱ����Դ�ĸ���
B��̼���Ϸ�����ԭ��Ӧ
C����Ƭ�ϵĵ缫��ӦʽΪ2Cl�D�D2e�� �� Cl2��
D����Ƭ�������ֵĻ�������Mg(OH)2
4��ѡ���� �ò��缫���һ��Ũ�ȵ��������ʵ�ˮ��Һ���ڵ���ĵ��Һ�м�����ˮ����ʹ��ҺŨ�Ȼָ������ǰŨ�ȵ��ǣ�?��
A��NaCl
B��Na2CO3
C��CuSO4
D��K2S
5������� ��8�֣���NaOH��Һ���������е�SO2�������õ�Na2SO3��Һ���е�⣬��ѭ������NaOH��ͬʱ�õ�H2SO4����ԭ������ͼ��ʾ��(�缫����Ϊʯī)
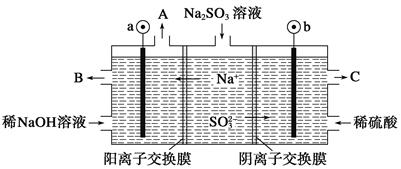
��1��ͼ��a��Ҫ���ӵ�Դ��(���������)________����C��������������________��
��2��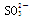 �ŵ�ĵ缫��ӦʽΪ________ ____�� �ŵ�ĵ缫��ӦʽΪ________ ____��
��3��������������������������ǿ����ƽ���ƶ�ԭ������ԭ��____ ____��
|