1��ѡ���� ��ͼ��X��Y�ֱ���ֱ����Դ��������ͨ�����a�������������ӣ�b�����崦����ɫ������ų���������һ������ǣ�?��
�ο��𰸣�A
���������ͨ�����a�������������ӣ�b�����崦����ɫ������ų�����˵��a�缫Ӧ������������Һ�еĽ��������ӷŵ硣b�缫����������Һ�е�OH���ŵ�������������˵��X�Ǹ�����Y������������ѡ��A���ϣ�B��û�н���������C�е缫���Ʋ���ȷ��D��������������ѡA��
�����������Ǹ߿��еij������ͣ������е��Ѷȵ����⡣�����ۺ���ǿ�����ض�ѧ������֪ʶ�Ĺ��̺�ѵ��������������ѧ�������������������ѧ��������û���֪ʶ���ʵ�����������������Ĺؼ�����ȷ���صĹ���ԭ����Ȼ��������������ü��ɡ�
�����Ѷȣ���
2��ѡ���� ��֪Ǧ���طŵ�ʱ�������·�Ӧ��������Pb��SO42-�D2e�D��PbSO4��������PbO2��4H����SO42-��2 e�D��PbSO4��2H2O����Ǧ���طŵ�ת�Ƶĵ���������Cl-�Ƶ�Cl2 22.4L�������ʱ����������ĵ���������ʵ���������?��?��
A��2.5 mol
B��2 mol
C��1 mol
D��5 mol
�ο��𰸣�B
�������������Ǧ���صĵ缫��Ӧ��֪����1mol����ת������1molH2SO4������״��������Cl2 22.4Lʱ��ת�Ƶ�����Ϊ2mol��������������2mol����ѡB��
������������Ҫ���ݵ����غ������㡣
�����Ѷȣ�һ��
3������� ��4�֣���ͼװ��B����Ũ�Ⱦ�Ϊ0.1mol/L��NaCl��CuSO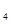 �����Һ����Һ���Ϊ500ml��M��N��Ϊʯī�缫����װ��A��Zn����������6.5gʱ��N����������____________g����ʱ�����е缫���ܹ��ռ���������������Ϊ___________L������ɱ�״���µ��������
�����Һ����Һ���Ϊ500ml��M��N��Ϊʯī�缫����װ��A��Zn����������6.5gʱ��N����������____________g����ʱ�����е缫���ܹ��ռ���������������Ϊ___________L������ɱ�״���µ��������

�ο��𰸣���1��3.2 ��2��4.76
���������AΪԭ���пΪ������ͬΪ������BΪ���أ�MΪ������NΪ������װ����ÿ���缫ת�Ƶ�������ȣ�A��Zn����������6.5gʱת�Ƶ���0.2mol��ͭ������������ת�Ƶ���0.2mol��������0.1mol��M�缫Ϊ������ת��0.2mol����ʱ���Ⱥ���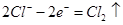 ��
��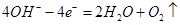 ����Һ�й���0.05mol NaCl,��������0.025mol����������0.0375 mol��N�缫Ϊ�������Ⱥ���
����Һ�й���0.05mol NaCl,��������0.025mol����������0.0375 mol��N�缫Ϊ�������Ⱥ���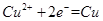 ��
��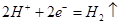 ����Һ�й���0.05mol CuSO
����Һ�й���0.05mol CuSO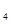 ������0.05mol Cu��0.05 mol���������Թ���������0.2125mol����״���µ����Ϊ4.76L��
������0.05mol Cu��0.05 mol���������Թ���������0.2125mol����״���µ����Ϊ4.76L��
���㣺���⿼����ء�ԭ����ۺϼ��㡣
�����Ѷȣ�һ��
4��ѡ���� ��̼���缫���һ��������ijŨ�ȵ��Ȼ�����Һ��һ��ʱ���ֹͣ��⡣��ʱ������100g 36.5%��Ũ���ᣬ������Һ������ԭ��Һ��ȫ��ͬ�����������ת�Ƶ��ӵ����ʵ���ԼΪ��������
A��9 mol
B��7 mol
C��6 mol
D��8 mol
�ο��𰸣�D
�����������
�����Ѷȣ�һ��
5��ѡ���� ���������ӡ��⡱ʳ�ν϶��ʹ���˵����(KIO3)��������ڹ�ҵ�Ͽ��õ�ⷨ��ȡ����ʯī�Ͳ����Ϊ�缫����KI��ҺΪ���Һ����һ�������µ�⣬��Ӧ�Ļ�ѧ����ʽΪ��KI��3H2O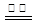 KIO3��3H2���������й�˵������ȷ���� �� ��
KIO3��3H2���������й�˵������ȷ���� �� ��
A�����ת��3 mol e��ʱ�������Ͽ��Ƶ�KIO3 107 g
B�����ʱ�� ʯī�������������������
C�����ʱ�������缫��Ӧʽ��I��?6e����3H2O = IO3����6H��
D���������е������Һ��pH��С