1、填空题 (共8分)
(1)(3分)有反应:2NO2 N2O4?△H<0,根据图像判断后填空:
N2O4?△H<0,根据图像判断后填空:
 ?t1? t2? t3? t4? t5? t6? t
?t1? t2? t3? t4? t5? t6? t
t1至t3采取的措施是_____________;t4至t5采取的措施是______________t6采取的措施是_________________。
(2)(3分)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学反应方程式:
①Fe2O3(s)+3CO(g)=2Fe(s)+3CO2?△H=-25kJ/mol
②3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g)?△H=-47kJ/mol
③Fe3O4(s)+CO(g)=3FeO(s)+CO2(g)?△H=+640kJ/mol
请写出FeO(s)被CO(g)还原成Fe和CO2(g)的热化学方程式?。
(3)(2分)下图表示800℃时,A、B、C三种气体物质的浓度随时间变化的情况,t是达到平衡状态的时间。则该反应的化学方程式为________________________。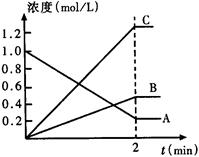
2、选择题 一密闭烧瓶中装有NO2气体,在一定条件下达到化学平衡2NO2 ?N2O4(正反应为放热反应)。将该烧瓶放在热水中,对现象的描述正确的是?
?N2O4(正反应为放热反应)。将该烧瓶放在热水中,对现象的描述正确的是?
A.颜色不变
B.颜色变浅
C.颜色加深
D.无法判断
3、计算题 把4 mol A和4 mol B混合放入容积为2L的密闭容器里,发生反应3A(g)+2B(g) x C(g)+2D(g),经5s后反应达平衡。在此5s内C的平均反应速率为0.1 mol・L-1・s-1,同时生成2 mol D。试计算:(1)达到平衡状态时B的转化率;
x C(g)+2D(g),经5s后反应达平衡。在此5s内C的平均反应速率为0.1 mol・L-1・s-1,同时生成2 mol D。试计算:(1)达到平衡状态时B的转化率;
(2)试算x的值;
(3)若温度和压强维持不变,当生成2 mol D时,此时容器内气体的体积是多少?
4、选择题 一定温度下,在2L 的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示。下列描述正确的是
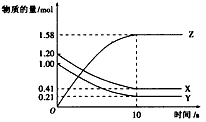
[? ]
A.反应开始到10 s,用Z表示的反应速率为0.158 mol・L-1・s-1
B.反应开始到 l0 s,X的物质的量浓度减少了0.79 mol・L-1
C.反应开始到10 s,Y的转化率为79.0%
D.反应的化学方程式为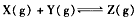
5、简答题 将4mol SO2与2mol O2放入4L的密闭容器中,在一定条件下反应达到平衡:2SO2(g)+O2(g)?2SO3(g),测得平衡时混合物总的物质的量为5mol,求:
(1)平衡时SO3的浓度;
(2)平衡时SO2的转化率.