|
|
|
高考化学知识点整理《电解池原理》在线测试(2019年最新版)(十)
2020-07-08 00:52:20
【 大 中 小】
|
1、选择题 Ⅰ.已知在常温常压下:
① 2CH3OH(l)十3O2(g)=2CO2(g)+4H2O(g) △H= -1275.6 kJ・mol―1
② H2O(l)=H2O(g) △H="+" 44.0 kJ.mo―1
写出表示甲醇燃烧热的热化学方程式 。
Ⅱ.磷酸(H3PO4)在水溶液中各种存在形式物质的量分数δ随pH的变化曲线如下图:
(1)在Na3PO4溶液中,c(Na+)/c(PO43-) 3(填“>”“=”“<”),向Na3PO4溶液中滴入稀盐酸后 ,pH从10降低到5的过程中发生的主要反应的离子方程式为 。
(2)从图中推断NaH2PO4溶液中各种微粒浓度大小关系正确的是 。(填选项字母)
A、C(Na+)> C(H2PO4 -)> C(H+)> C(HPO4 2-)> C(H3PO4 )
B、C(Na+)> C(H2PO4 -)> C(OH-)> C( H3PO4)> C(HPO4 2- )
C、C(H+)+ C(Na+)=C(OH-)+C(H2PO4-)+2C(HPO42-)+3C(PO43-)+C(H3PO4 )
D、C(Na+)=C(H2PO4-)+C(HPO42-)+C(PO43-)+C(H3PO4 )
(3)假设25℃条件下测得0.1 mol・L
参考答案:
本题解析:
本题难度:困难
2、选择题 已知在pH为4-5的溶液中,Cu2+几乎不水解,而Fe3+几乎完全水解。某学生拟用电解CuSO4溶液的方法测定铜的相对原子质量。该同学向pH=3.8的含有Fe2(SO4)3杂质的CuSO4溶液中加入适量的黑色粉末X,充分搅拌后过滤,将滤液用如下图所示装置电解,其中某电极增重ag,另一电极上产生标准状况下的气
VmL。下列说法正确的是

[? ]
A.黑色粉末X是铁粉
B.铜电极连接电源正极
C.石墨电极上发生的反应是4OH--4e-=O2↑+2H2O
D.铜的相对原子质量的计算式是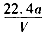
参考答案:C
本题解析:
本题难度:一般
3、填空题 某课外小组分别用下图所示装置对原电池和电解池原理进行实验探究。
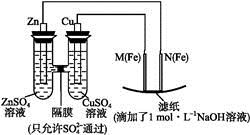 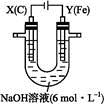
图1 图2
请回答:
Ⅰ.用图1所示装置进行第一组实验。
(1)在保证电极反应不变的情况下,不能替代Cu作电极的是 (填序号)。
A.铝
B.石墨
C.银
D.铂
| (2)N极发生反应的电极反应为 。
(3)实验过程中,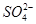 (填“从左向右”“从右向左”或“不”)移动;滤纸上能观察到的现象有 。 (填“从左向右”“从右向左”或“不”)移动;滤纸上能观察到的现象有 。
Ⅱ.用图2所示装置进行第二组实验。实验过程中,两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清。查阅资料发现,高铁酸根(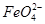 )在溶液中呈紫红色。 )在溶液中呈紫红色。
(4)电解过程中,X极区溶液的pH (填“增大”“减小”或“不变”)。
(5)电解过程中,Y极发生的电极反应为Fe-6e-+8OH- 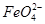 +4H2O和 。 +4H2O和 。
(6)若在X极收集到672 mL气体,在Y极收集到168 mL气体(均已折算为标准状况下的气体体积),则Y电极(铁电极)质量减少 g。
(7)在碱性锌电池中,用高铁酸钾作为正极材料,电池反应为:
2K2FeO4+3Zn Fe2O3+ZnO+2K2ZnO2 Fe2O3+ZnO+2K2ZnO2
该电池正极发生的反应的电极反应为 。
参考答案:
(1)A (2)2H++2e- H2↑(或2H2O+2e- H2↑(或2H2O+2e- H2↑+2OH-) H2↑+2OH-)
(3)从右向左 滤纸上M极附近有红褐色斑点产生(答出“红褐色斑点”或“红褐色沉淀”即可)
(4)增大 (5)4OH--4e- 2H2O+O2↑ 2H2O+O2↑
(6)0.28 (7)2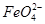 +6e-+5H2O +6e-+5H2O Fe2O3+10OH- Fe2O3+10OH-
本题解析:
(1)铝与CuSO4溶液反应,且比Zn活泼;(2)N极为阴极,发生得电子反应,溶液中只有H+得电子;(3)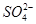 向负极(左)移动,滤纸上阴极有OH-生成、阳极有Fe2+生成,两离子生成白色Fe(OH)2沉淀,迅速变为灰绿色,最后变为红褐色;(4)X极是阴极,H+得电子,所以pH增大;(5)两极均有气体产生,可知阳极生成的气体只能是氧气;(6)X极收集n(H2)="0.03" mol,得0.06 mol电子,Y极收集n(O2)="0.007" 5 mol,OH-失去0.03 mol电子,所以参加反应的n(Fe)= 向负极(左)移动,滤纸上阴极有OH-生成、阳极有Fe2+生成,两离子生成白色Fe(OH)2沉淀,迅速变为灰绿色,最后变为红褐色;(4)X极是阴极,H+得电子,所以pH增大;(5)两极均有气体产生,可知阳极生成的气体只能是氧气;(6)X极收集n(H2)="0.03" mol,得0.06 mol电子,Y极收集n(O2)="0.007" 5 mol,OH-失去0.03 mol电子,所以参加反应的n(Fe)=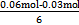 ="0.005" mol;(7)第一步,标化合价看化合价变化:铁的化合价降低3价;第二步,依据得失电子写2 ="0.005" mol;(7)第一步,标化合价看化合价变化:铁的化合价降低3价;第二步,依据得失电子写2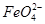 +6e- +6e-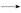 Fe2O3;第三步,依据电荷守恒,结合电解质溶液显碱性配平得电极反应:2 Fe2O3;第三步,依据电荷守恒,结合电解质溶液显碱性配平得电极反应:2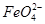 +6e-+5H2O +6e-+5H2O Fe2O3+10OH-。 Fe2O3+10OH-。
本题难度:困难
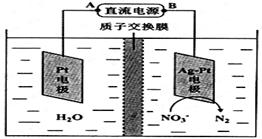
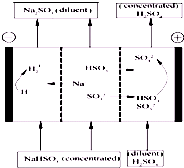
4、选择题 某研究小组用NaOH溶液吸收二氧化硫,将所得的混合液进行电解循环再生,这种新工艺叫再生循环脱硫法.其中阴阳膜组合循环再生机理如图,则下列有关说法错误的是( )
A.阳极区酸性增强
B.阴极区电极反应式为:2H++2e-=H2↑
C.diluent和concentrated的中文含义为浓缩的、稀释的
D.该过程中的副产品主要为H2SO4
|
参考答案:A、电解池中,阳极不是活泼电极时,放电的是氢氧根,浓度减小,所以氢离子浓度增大,酸性增强,故A正确;
B、电解池中,阴极区是溶液中的氢离子放电,电极反应式为:2H++2e-=H2↑,故B正确;
C、diluent和concentrated的中文含义为稀释的、浓缩的,故C错误.
D、亚硫酸根具有较强的还原性,易被氧化为硫酸根,该过程中的副产品主要为H2SO4,故D正确.
故选C.
本题解析:
本题难度:简单
5、填空题 用铂电极电解氢氧化钠溶液,测定两极逸出气体的体积,记录如下
时间/min气体体积/L
| 1
| 2
| 3
| 4
| 5
| 6
| 7
| 8
|
阴极生成的气体
| 6
| 12
| 20
| 29
| 39
| 49
| 59
| 69
|
阳极生成的气体
| 2
| 4
| 7
| 11
| 17
| 23
| 28
| 34
|
(1)完成有关的电极反应式:阴极__________;阳极____________;
(2)完成电解的总化学方程式_______________________________;
(3)开始电解阶段两极产生气体的体积比不符合理论比值的原因是______________________;
(4)自第__________分钟起阴极与阳极产生气体的体积比约为理论的比值;
(5)该过程NaOH溶液的pH如何变化__________________________________。
参考答案:(1)4H++4e-====2H2↑? 4OH--4e-====2H2O+O2↑?(2)2H2O 2H2↑+O2↑
2H2↑+O2↑
(3)开始阶段H2、O2在水中未达到饱和,H2在水中溶解度比O2的溶解度小
(4)4?(5)逐渐增大
本题解析:电解NaOH溶液相当于电解水,但随着水量的减少,NaOH浓度逐渐增大。
本题难度:简单
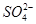 (填“从左向右”“从右向左”或“不”)移动;滤纸上能观察到的现象有 。
(填“从左向右”“从右向左”或“不”)移动;滤纸上能观察到的现象有 。 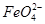 )在溶液中呈紫红色。
)在溶液中呈紫红色。
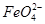 +4H2O和 。
+4H2O和 。  Fe2O3+ZnO+2K2ZnO2
Fe2O3+ZnO+2K2ZnO2
 2H2↑+O2↑
2H2↑+O2↑