1、选择题 下列关于电子云的说法,正确的是( )
A.电子云的每一个小黑点代表一个电子
B.小黑点密表示在该核外空间的电子数多
C.小黑点密表示在该核外空间的单位体积内电子出现的概率大
D.小黑点是表示电子绕核作高速圆周运动
参考答案:C
本题解析:
本题难度:简单
2、选择题 下列关于氢原子电子云图的说法正确的是( )
A.通常用小黑点来表示电子的多少,黑点密度大,电子数目大
B.黑点密度大,单位体积内电子出现的机会大
C.通常用小黑点来表示电子绕核作高速圆周运动
D.电子云图是对运动无规律性的描述
参考答案:B
本题解析:
本题难度:一般
3、简答题 A、B、C、D、E五种短周期元素,原子序数依次增大,A、E同主族,A元素的原子半径最小,B元素原子的最外层电子数是内层电子数的2倍,C元素原子的电子层数为n,最外层电子数为2n+1,A、B、C、E每种元素都能与D元素组成两种或两种以上的常见化合物.回答下列问题:
(1)写出下列各元素的名称:A______?D______
(2)上述五种元素中,第一电离能最小的元素是______,基态原子未成对电子数最多的原子核外电子排布式为______.
(3)已知:BA3DA(g)+A2D(g)=BD2(g)+3A2(g)△H1=+49.0kJ/mol,BA3DA(g)+1/2D2(g)=BD2(g)+2A2(g)△H2=-192.9kJ/mol,试写出:气态BA3DA完全燃烧生成气态A2D的热化学方程式(用推出的元素符号书写);______
(4)对可逆反应3A2(g)+C2(g)?2CA3(g)当反应达到平衡位置时不断改变条件(不改变A2、C2和CA3的量),右图表示反应速率与反应过程的关系,其中表示平衡混合物中CA3的含量最高的一段时间是______.在一定温度下,若将4amol?A2和2a?mol?C2放入lL的密闭容器中,充分反应后测得C2的转化率为50%,则该反应的平衡常数为______.若此时再向该容器中投入a?mol?A2,a?mol?C2利2a?mol?CA3,判断平衡移动方向______(“正”“逆”或“不移动”).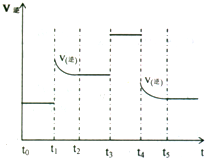
参考答案:A原子半径最小,则A为H元素;B元素原子的最外层电子数是内层电子数的2倍,则B为C元素;C元素原子的电子层数为n,最外层电子数为2n+1,当n为2时,C为N元素,当n为3时,C为Cl元素,根据题意C不能为Cl,否则E就不是短周期元素,所以C为N元素;A、E同主族,所以E为Na元素;A、B、C、E每种元素都能与D元素组成两种或两种以上的常见化合物,则D为O元素.
(1)由以上推断可知A为H元素,D为O元素,按要求写元素名称为:氢 氧,故答案为:氢? 氧;
(2)根据第一电离能变化规律,周期表中,同周期从左到右,电离能逐渐增大,同主族从上到下,第一电离能逐渐减小,所以这五种元素中钠的第一电离能最小.
H、C、N、O、Na这五种元素的未成对电子依次为:1、2、3、2、1,N元素的未成对电子数最多,电子排布式为:1s22s22p3.故答案为:Na? 1s22s22p3;
(3)把字母换成具体元素得:①CH3OH(g)+H2O(g)=CO2(g)+3H2(g);△H=+49.0kJ?mol-1
②CH3OH(g)+12O2(g)=CO2(g)+2H2(g);△H=-192.9kJ?mol-1
根据盖斯定律将②×3-①×2可得:CH3OH(g)+32 O2(g)=CO2(g)+2H2O(l)
△H=-192.9kJ/mol×3-49kJ/mol×2=-676.7kJ/mol,
故答案为:CH3OH(g)+32 O2(g)=CO2(g)+2H2O(l)△H=-676.7kJ/mol;
(4)从图象可看出,改变条件平衡一直向逆反应方向移动,故t0-t1 NH3含量最高.
? ?3H2+N2=2NH3
起始浓度(mol/L)? 4 a? 2a? 0?
转化浓度(mol/L)?3a? a? 2a
平衡浓度(mol/L)? a? a? 2a
K=(2a)2a×a3=4a2.若此时再向该容器中投入a?mol?A2,a?mol?C2和2a?mol?CA3时,
相当于加压,平衡向体积减少方向即正向移动.故答案为:t0-t1 4a2正.
本题解析:
本题难度:一般
4、填空题 第四周期第六个元素的电子构型是_________________。
参考答案:
1s22s22p63s23p63d54s1
本题解析:
本题难度:一般
5、填空题 生物质能是一种洁净、可再生的能源.生物质气(主要成分为CO、CO2、H2等)与H2混合,催化合成甲醇是生物质能利用的方法之一.
(1)上述反应的催化剂含有Cu、Zn、Al等元素.写出基态Zn原子的核外电子排布式______.
(2)根据等电子原理,写出CO分子结构式______.
(3)甲醇催化氧化可得到甲醛,甲醛与新制Cu(OH)2的碱性溶液反应生成Cu2O沉淀.
①甲醇的沸点比甲醛的高,其主要原因是______;甲醛分子中碳原子轨道的杂化类型为______.
②甲醛分子的空间构型是______;1mol甲醛分子中σ键的数目为______.
③在1个Cu2O晶胞中(结构如图1所示),所包含的Cu原子数目为______.
(4)元素Cu的一种氯化物晶体的晶胞结构如图2所示,该氯化物的化学式是______,它可与浓盐酸发生非氧化还原反应,生成配合物HnCuCl3,反应的化学方程式为______.
参考答案:(1)Zn的原子序数为30,注意3d轨道写在4s轨道的前面,电子排布式为1s22s22p63s23p63d104s2或[Ar]3d104s2,
故答案为:1s22s22p63s23p63d104s2或[Ar]3d104s2;
(2)依据等电子原理,可知CO与N2为等电子体,N2分子的结构式为:N≡N,互为等电子体分子的结构相似,可写出CO的结构式为C≡O,故答案为:C≡O;
(3)①甲醇分子之间形成了分子间氢键,甲醛分子间只是分子间作用力,而没有形成氢键,故甲醇的沸点高,甲醛分子中含有碳氧双键,故碳原子轨道的杂化类型为sp2杂化,故答案为:甲醇分子之间形成氢键;sp2杂化;
?②甲醛为sp2杂化,不含孤电子对,分子的空间构型为平面三角形;1mol甲醛分子中含有2mol碳氢δ键,1mol碳氧δ键,故含有δ键的物质的量为3mol,数目为3NA个;
故答案为:平面三角形;3NA;
③依据晶胞示意图可以看出Cu原子处于晶胞内部,所包含的Cu原子数目为4,故答案为:4;
(4)由晶胞可知Cu原子位于晶胞内部,含有4个Cu,Cl位于顶点和面心,共含有8×18+6×12=4,则氯化物的化学式是CuCl,它可与浓盐酸发生非氧化还原反应,生成配合物HnCuCl3,则应需要2HCl,
则反应的化学方程式为CuCl+2HCl=H2CuCl3.
故答案为:CuCl;CuCl+2HCl=H2CuCl3.
本题解析:
本题难度:一般