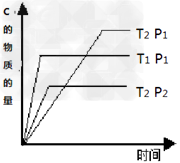
1、选择题 投入一定量的物质A和B发生可逆反应:2A(g)+nB(g) mC(g)?,在温度分别为T1、T2,压强分别为P1、P2的条件下,测得C的物质的量与时间的关系如图所示,?有关该反应的说法正确的是
mC(g)?,在温度分别为T1、T2,压强分别为P1、P2的条件下,测得C的物质的量与时间的关系如图所示,?有关该反应的说法正确的是
[? ]
A.?n+2<m?该反应正反应为放热反应
A.?n+2<m?该反应正反应为吸热反应
C.?n+2>m?该反应正反应为放热反应
D.?n+2>m?该反应正反应为吸热反应
2、选择题 下列可逆反应达平衡后,升高温度可使混和气体的平均相对分子质量减小的是( )
A.N2(g)+3H2(g)

2NH3(g)放热反应
B.H2(g)+I2(g)

2HI(g)放热反应
C.A(g)+B(g)

3C(g)放热反应
D.4NH3(g)+5O2(g)

4NO(g)+6H2O(g)放热反应
3、填空题 (12分)为了减少CO对大气的污染,某研究性学习小组拟研究CO和H2O反应转化为绿色能源H2。已知:2CO(g)+O2(g)=2CO2(g) ΔH=-566kJ・moL-1
2H2(g)+O2(g)=2H2O(g) ΔH=-483.6KJ・moL-1
H2O (g)=H2O(l) ΔH=-44.0KJ・moL-1
(1)氢气的燃烧热△H= 。
(2)写出CO和H2O(g)作用生成CO2和H2的热化学方程式 。
(3)往1L体积不变的容器中加入1.00mol CO和1.00mol H2O(g),在t℃时反应并达到平衡,若该反应的化学平衡常数K=1,则t℃时CO的转化率为 ;反应达到平衡后,升高温度,此时平衡常数将 (填“变大”、“不变”或“变小”),平衡将向 (填“正”或“逆”)反应方向移动。
(4)为了提高CO的转化率,可采取的措施是 。
A.增大的CO浓度
B.增大H2O(g) 的浓度
C.使用催化剂
D.降低温度