1、填空题 (1)已知:25℃时,一些弱电解质的电离常数如下:NH3・H2O:1.77×10―5? H2CO3:4.3×10―7(第一步电离)。则:NH4HCO3溶液显?性 。
(2)物质的量浓度相同的醋酸和氢氧化钠溶液混合后,溶液中醋酸根离子和钠离子浓度相等,则混合后溶液呈?性,醋酸体积?(填“>”、“<”、“=”)氢氧化钠溶液体积。
(3)电解质A的化学式为NanB,测得浓度为c mol/L的A溶液的pH=10,A溶液呈碱性的原因是(用离子方式程式表示)________________
(4)污水中含有Hg2+,用难溶的FeS作为沉淀剂可使Hg2+转化为HgS而除去,该反应能进行的依据是:?;有人认为加入FeS作为沉淀剂还可以起到净化水的作用,请您运用所学知识解释?
(5)已知Ksp(AB2)=4.2×10-8,Ksp(AC)=3.0×10―15。在AB2、AC均为饱和的混合液中,测得c(B―)=1.6×10―3 mol・L-1,则溶液中c(C2―)为?mol/L。
参考答案:(1)(1分)碱
(2)(1分)中性,(1分)>
(3)(2分)Bn-+H2O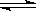 HB(n-1)-+OH-
HB(n-1)-+OH-
(4)Ksp(HgS)<Ksp(FeS);因发生Hg2++FeS=HgS+Fe2+,产生的Fe2+可被氧化为Fe3+,Fe3+水解形成Fe(OH)3胶体,吸附杂质而净化水(每空2分,共4分)
(5)(2分)1.83×10―13
本题解析:(1)NH3・H2O:1.77×10―5? H2CO3:4.3×10―7(第一步电离),这说明了碳酸氢根离子的水解程度比铵根离子更加弱,所以其水解程度较大,故NH4HCO3溶液显碱性;2)物质的量浓度相同的醋酸和氢氧化钠溶液混合后,溶液中醋酸根离子和钠离子浓度相等,根据电荷守恒可以得到:c(CH3COO-)+ c(OH-)=c(Na+)+ c(H+),因为c(CH3COO-)=c(Na+),所以 c(OH-)=c(H+),故混合后溶液呈中性,醋酸体积>氢氧化钠溶液体积;(3)电解质A的化学式为NanB,测得浓度为c mol/L的A溶液的pH=10,说明了B离子发生了水解,其离子方程式为Bn-+H2O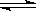 HB(n-1)-+OH-;(4)污水中含有Hg2+,用难溶的FeS作为沉淀剂可使Hg2+转化为HgS而除去,该反应能进行的依据是:Ksp(HgS)<Ksp(FeS);FeS作为沉淀剂还可以起到净化水的作用,其原因为因发生Hg2++FeS=HgS+Fe2+,产生的Fe2+可被氧化为Fe3+,Fe3+水解形成Fe(OH)3胶体,吸附杂质而净化水;(5)因为Ksp(AB2)=4.2×10-8,Ksp(AC)=3.0×10―15,c(B―)=1.6×10―3 mol・L-1,AB2、AC均为饱和的混合液,即c2(B―)c(A―)=4.2×10-8,所以c(A2+)=1.64×10―2mol・L-1,
HB(n-1)-+OH-;(4)污水中含有Hg2+,用难溶的FeS作为沉淀剂可使Hg2+转化为HgS而除去,该反应能进行的依据是:Ksp(HgS)<Ksp(FeS);FeS作为沉淀剂还可以起到净化水的作用,其原因为因发生Hg2++FeS=HgS+Fe2+,产生的Fe2+可被氧化为Fe3+,Fe3+水解形成Fe(OH)3胶体,吸附杂质而净化水;(5)因为Ksp(AB2)=4.2×10-8,Ksp(AC)=3.0×10―15,c(B―)=1.6×10―3 mol・L-1,AB2、AC均为饱和的混合液,即c2(B―)c(A―)=4.2×10-8,所以c(A2+)=1.64×10―2mol・L-1,
c(C2―)=Ksp(AC)/c(A2+)=3.0×10―15/1.64×10―2=1.83×10―13mol・L-1。
点评:本题考查了盐类水解,电荷守恒、溶度积的计算,这些知识是高考考查的重点和难点,本题有一定的综合性,难度适中。
本题难度:一般
2、填空题 (16分)广东省有着丰富的海洋资源。海水提取食盐和Br2以后的盐卤可以用来制备纯净的MgCl2或MgO。盐卤中含有Mg2+、Cl-,还含有少量Na+、Fe2+、Fe3+、SO42-等。制备流程如下图
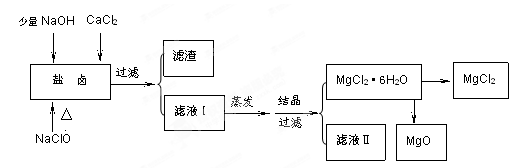
(1)滤液Ⅱ中所含主要的杂质离子是?(写离子符号)。
(2) 加入NaClO的作用是?。
(3)温度和压强P(HCl)g对MgCl2・6H2O晶体热分解产物的影响如图所示。
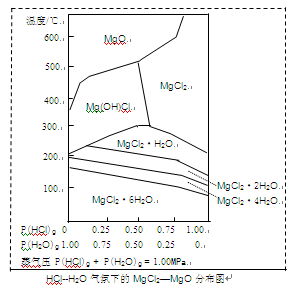
请回答下列问题:
①写出P(HCl)g = 0.25MPa,温度从300℃升高到550℃时反应的化学方程式?;
②实际生产中,将MgCl2・6H2O晶体加热到600℃的过程中几乎得不到无水MgCl2,其原因是
?;若要得到无水MgCl2须采取的措施是?。
参考答案:(1)Na+
(2)将Fe2+ 氧化为 Fe3+ ,并形成Fe(OH)3 被除去
(3)① Mg(OH)Cl  ?MgO? + HCl↑
?MgO? + HCl↑
②P(HCl)小,加热时Mg2+?会发生水解
通入HCl,增大P(HCl,抑制 Mg2+水解
本题解析:
(1)滤渣的成分是Fe(OH)3;滤液Ⅱ中所含的主要杂质离子是Na+。 (2)加入NaClO还能起到的作用是氧化Fe2+使它变成Fe(OH)3沉淀而除去。 (3)直接将MgCl2・6H2O加强热能得到MgO,反应的化学方程式是MgCl2・6H2O MgO+2HCl↑+5H2O↑。用MgCl2・6H2O制备无水MgCl2过程中为抑制上述反应,所需要的化学试剂是HCl气体。
MgO+2HCl↑+5H2O↑。用MgCl2・6H2O制备无水MgCl2过程中为抑制上述反应,所需要的化学试剂是HCl气体。
① Mg(OH)Cl  ?MgO? + HCl↑②P(HCl)小,加热时Mg2+?会发生水解;通入HCl,增大P(HCl,抑制 Mg2+水解。
?MgO? + HCl↑②P(HCl)小,加热时Mg2+?会发生水解;通入HCl,增大P(HCl,抑制 Mg2+水解。
本题难度:一般
3、选择题 物质的量浓度相同的一元强碱和一元强酸相互反应时,溶液
A.呈酸性
B.呈碱性
C.呈中性
D.酸碱性无法判断
参考答案:D
本题解析:略
本题难度:一般
4、选择题 下列关于各溶液的描述中正确的是? ( )。
A.pH相等的①NH4Cl,②(NH4)2SO4,③NH4HSO4的溶液中,c(NH4+)大小:①=②=③
B.常温下,在10 mL pH=12的氢氧化钠溶液中加入pH=2的HA至pH刚好等于7,所得溶液体积V(总)≤20 mL
C.向1.00 L 0.3 mol・L-1的NaOH溶液中缓慢通入CO2气体至溶液增重8.8 g,所得溶液中:3c(Na+)=2[c(HCO3―)+c(CO32―)+c(H2CO3)]
D.浓度均为0.1 mol・L-1的CH3COOH和CH3COONa溶液等体积混合:c(CH3COO-)-c(CH3COOH)=c(H+)-c(OH-)
参考答案:B
本题解析:NH4Cl,(NH4)2SO4溶液中NH4+水解使溶液呈酸性:NH4++H2O NH3・H2O+H+,但水解是微弱的,NH4HSO4=NH4++H++SO42―,H+全部电离,溶液呈酸性,故c(NH)相同的NH4Cl,(NH4)2SO4,NH4HSO4三溶液中,c(H+)大小:①=②<③,现三溶液pH相同,则c(NH4+)大小:①=②>③,A项错误;若HA为强酸,则等体积混合时,pH恰好等于7,V(总)=20 mL,若HA为弱酸,HA部分电离出H+,要使混合后溶液呈中性,则酸的体积必须小于10 mL,V(总)<20 mL,B项正确;0.3 mol NaOH与0.2 mol CO2反应:3NaOH+2CO2=Na2CO3+NaHCO3+H2O,所得溶液为等浓度的Na2CO3和NaHCO3混合液,溶液中n(Na)∶n(C)=3∶2,据此得物料守恒式:2c(Na+)=3[c(HCO3―)+c(CO32―)+c(H2CO3)],C项错误;等浓度的CH3COOH与CH3COONa的混合溶液中存在电荷守恒式:c(Na+)+c(H+)=c(OH-)+c(CH3COO-),故c(H+)-c(OH-)=c(CH3COO-)-c(Na+),D项错误。
NH3・H2O+H+,但水解是微弱的,NH4HSO4=NH4++H++SO42―,H+全部电离,溶液呈酸性,故c(NH)相同的NH4Cl,(NH4)2SO4,NH4HSO4三溶液中,c(H+)大小:①=②<③,现三溶液pH相同,则c(NH4+)大小:①=②>③,A项错误;若HA为强酸,则等体积混合时,pH恰好等于7,V(总)=20 mL,若HA为弱酸,HA部分电离出H+,要使混合后溶液呈中性,则酸的体积必须小于10 mL,V(总)<20 mL,B项正确;0.3 mol NaOH与0.2 mol CO2反应:3NaOH+2CO2=Na2CO3+NaHCO3+H2O,所得溶液为等浓度的Na2CO3和NaHCO3混合液,溶液中n(Na)∶n(C)=3∶2,据此得物料守恒式:2c(Na+)=3[c(HCO3―)+c(CO32―)+c(H2CO3)],C项错误;等浓度的CH3COOH与CH3COONa的混合溶液中存在电荷守恒式:c(Na+)+c(H+)=c(OH-)+c(CH3COO-),故c(H+)-c(OH-)=c(CH3COO-)-c(Na+),D项错误。
本题难度:一般
5、选择题 下列溶液中有关粒子的物质的量浓度关系正确的是?(?)
A.氯水中:2c(Cl2)=c(ClO-)+c(Cl-)+c(HClO)
B.25℃时,pH=12的NaOH溶液与pH=12的氨水中:c(Na+)=c(NH4+)
C.pH=4的0.1 mol・L-1的NaHA溶液中:c(HA-)>c(H+)>c(H2A)>c(A2-)
D.等物质的量的Na2CO3、NaHCO3的混合溶液中:
c(CO32-)+2c(OH-)=c(HCO3-)+c(H2CO3)+2c(H+)
参考答案:C
本题解析:略
本题难度:简单