| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学知识点整理《物质结构和元素周期律》高频试题预测(2019年最新版)(二)
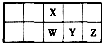 参考答案:根据元素周期表在周期表中的物质可知,X处于第二周期,W、Y、Z处于第三周期,W、Y、Z在周期表中位置相邻,且X、W至少为第ⅢA族, 本题解析: 本题难度:一般 4、选择题 短周期元素中,原子基态时具有1个未成对电子的元素共有多少种: 参考答案:C 本题解析:H 1s1,Li 1s22s1,B 1s22s22p1,O 1s22s22p4,Na 1s22s22p63s1,Al 1s22s22p63s23p1,Cl? 1s22s22p63s23p4。共7种。 本题难度:一般 5、简答题 下表是元素周期表中短周期元素的一部分,表中所列字母分别代表一种元素(除注明外用化学用语空).
(2)D和G的气态氢化物稳定性比较:?>?; (3)在上述元素中其最高价氧化物对应水化物酸性最强的酸为?; (4)现有上表中所列字母代表的某一种元素,其单质通入到紫色石蕊溶液中的现象为先变红后褪色,该元素在周期表中位于第?周期,第?族; (5)“神舟”七号载人飞船内需要有一种化合物来吸收航天员呼出的CO2,你认为该物质应该是由上表中的(填字母序号)?元素组成的,用化学方程式表示吸收原理:?. 参考答案:根据元素周期表中元素的分布知识,可以知道A是H,B是He,D是C,E是N,F是O,C是Na,G是Si,H是Cl. 本题解析: 本题难度:一般 |
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高中化学知识点归纳《氧化性和还.. | |