1��ѡ���� ͨ����ʵ��Ĺ۲졢�����������ó���ȷ�Ľ����ǻ�ѧѧϰ����Ҫ����֮һ��������ʵ����ʵ������Ľ�����ȷ����
A��KI������Һ��ͨ��Cl2����Һ����ԭ���ǵ�������Cl2������ɫ��Ӧ
B��Ũ�����ڹ��������±��������Ũ����ȶ���������ɫ����������Ũ����
C��ij��Һ�м��������ữ���Ȼ�����Һ���а�ɫ��������˵������Һ�к���SO42-
D�������£�Ũ����ɴ��������ʻ�����������˵����������������Ũ�����Ӧ
�ο��𰸣�B
�����������������ǿ�����ԣ���KI�������ɵ��ʵ⣬������������ɫ��Ũ����ȶ������ֽ�����NO��NO2��H2O��NO2����ˮʹ����ʻ�ɫ����Һ�м��������ữ���Ȼ�����Һ���а�ɫ�������ɣ�����������AgCl��BaSO4������������������Ũ�����з����ۻ����ۻ����ڻ�ѧ�仯������B��
�����Ѷȣ�һ��
2������� ��A��B��C��D��E��ƿ����Һ���ֱ���HCl��BaCl2��NaHSO4��Na2CO3��AgNO3�е�һ�֣���֪����A��B��Ӧ���������ɣ���B��C��Ӧ�г������ɣ���C��D��Ӧ�г������ɣ���D��E��Ӧ�г������ɣ���A��E��Ӧ���������ɣ����ڢں͢۵ķ�Ӧ�����ɵij�����ͬһ�����ʣ�����գ�
��1���ڢں͢۵ķ�Ӧ�У����ɵij������ʵĻ�ѧʽ��______��
��2��A��______��B��______��C��______��D��______��E��______��
��3��A��E��Ӧ�����ӷ���ʽ��______��
�ο��𰸣����ݢޡ��ڢں͢۵ķ�Ӧ�����ɵij�����ͬһ�����ʡ���һ��Ϣ��֪��B��D�б�Ȼ������ͬ�����ӣ������ƶϳ�������HCl��BaCl2�������������ӷ�Ӧ����AgCl��������ˣ�C��Ȼ��AgNO3���ٸ��ݢ٣�A��B��Ӧ���������ɣ��ƶ�Bһ����HCl����ô��D��BaCl2��A��Na2CO3��ʣ���һ�����ʣ���NaHSO4����E��
��1�������Ϸ�����֪�ڢں͢۵ķ�Ӧ�У����ɵij���������AgCl���ʴ�Ϊ��AgCl��
��2�������Ϸ�����֪A��Na2CO3��B��HCl��C��AgNO3��DBaCl2��E��NaHSO4��
�ʴ�Ϊ��Na2CO3��HCl��AgNO3��BaCl2��NaHSO4��
��3��Na2CO3��NaHSO4��Ӧ����CO2��H2O����Ӧ�����ӷ���ʽ��2H++CO32-�TCO2��+H2O���ʴ�Ϊ��2H++CO32-�TCO2��+H2O��
���������
�����Ѷȣ�һ��
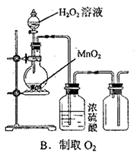
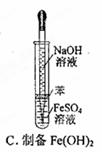
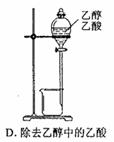
3��ѡ���� ��ͼ��ʾ���Լ�ѡ�û�ʵ�������ȷ����
 ?
? ?
? ?
?
�ο��𰸣�C
���������A�����Ը��������ҺӦ��ʢ������ʽ�ζ����У�A����ȷ���������ܶȴ��ڿ����ģ�Ӧ���������ſ������ռ���B����ȷ�������������������ױ��������������Ʊ�����������ʱ�ιܿ��Բ��뵽��Һ�У�C��ȷ���Ҵ��������ǻ��ܵģ������÷�Һ�����룬��Ӧ��������D����ȷ����ѡC��
��������ѧʵ�鳣��������ʹ�÷����ͻ�ѧʵ����������ǽ��л�ѧʵ��Ļ������Ի�ѧʵ��Ŀ����벻����ѧʵ��Ļ������������Ը���������Ҫ���Գ���������ѡ�á�ʵ���������Ϊ���ģ�ͨ����ʲô��Ϊʲô���������ص㿼��ʵ����������Ĺ淶�Ժ�ȷ���������֪ʶ���ʵ�������������
�����Ѷȣ���
4��ѡ���� ���л�ѧʵ����ʵ������Ͷ���ȷ����?
A����ΪKsp(CaCO3)��Ksp(CaSO4)�����Կ���Na2CO3��HCl��ȥˮ���е�CaSO4
B����п��ϡ���ᷴӦ�������ȴ�п�죬����Ϊ��п�ȴ�п��ԭ��ǿ
C�����з�̪��̼��������Һ��dz��ɫ���Ⱥ��ɫ�������Ϊ̼�����Ʒֽ�������̼����
D����������ˮ�з�����Ӧ�����ӷ���ʽΪS2 �C+ 2H2O H2S + 2OH �C
H2S + 2OH �C
�ο��𰸣�A
���������B�ԭ��Ӧ���Ǵ�п���γ���ԭ��أ��ʴ���C�ԭ��Ӧ����̼������ˮ��ʼ��ԣ��ʴ���D������ˮ���Ƿֲ����еģ��ʴ�����ѡA��
���������⿼���Ϊ�ۺϣ��漰�����ܵ���ʵij����ܽ�ƽ�⣬����ԭ������Һ��ɫ��ԭ����ע�����֪ʶ�Ļ��ۡ�
�����Ѷȣ���
5��ѡ���� ����9ͼ��ʾ��ʵ���У��ܴﵽʵ��Ŀ�ĵ���
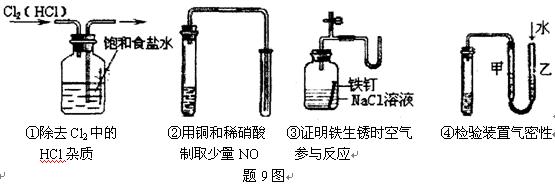
A���٢ڢۢ�
B���ڢۢ�
C���ۢ�
D���٢�
�ο��𰸣�C
�����������
�����Ѷȣ�һ��