1���ƶ��� W��X��Y��Z��ԭ���������������ͬһ��ͬ�ڵ�����Ԫ�ء�W��X�ǽ���Ԫ�أ�Y��Z�Ƿǽ���Ԫ�ء�Y�����������ִ���ѧ��������Ʒ�Ļ���ԭ�ϡ�
��ش�
��1��YԪ��ԭ�ӽṹʾ��ͼ____________ ��
��2����Z����ͨ��ˮ�У��ɵõ�����Ư�����õ���Һ����д����Ӧ�����ӷ���ʽ��______________ ��
��3��0.5 mol X����������W������������Ӧˮ�������Һ������Ӧ������������������״����Ϊ___________ ��
��4��WZ�������г������Σ�ʵ���Ҽ�������������ӵIJ�������������Ϊ��ȡ����WZ��������ˮ���μ�ϡ�������������Һ����������ɫ��������֤��WZ���и������ӡ���д����Ӧ�����ӷ���ʽ��_____________��
�ο��𰸣���1��
��2��Cl2 + 2H2O ==Cl- + H+ + HClO
��3��16.8 L
��4��Ag++Cl-==AgCl��
���������
�����Ѷȣ�һ��
2��ʵ���� ��9�֣���ˮ�Ȼ����ǰ�ɫ���壬������ˮ�֣���178��������װ����ˮ�Ȼ������Լ�ƿ�����ڳ�ʪ�����У����Զ���ը�����������������Ȼ�������Ϊ�л��ϳɺ�ʯ��ҵ�Ĵ����������ڴ������͵ȡ���ҵ���ɽ��������������û�����ˮ�Ȼ������������ڽ����������Ƶá�






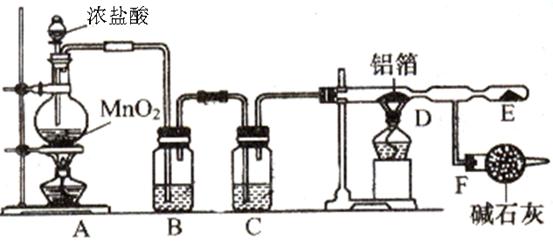
ij������ȤС����ʵ�����У�ͨ����ͼװ����ȡ������������ˮ�Ȼ�����
 ?
?
��1��Aװ���з�����Ӧ�Ļ�ѧ����ʽΪ?��
��2��B��Cװ����Ӧʢ�ŵ��Լ����Ʒֱ�Ϊ?��?��
��3����Aװ�õ�����������������B��Cװ�ö�ֱ�ӽ���D�ܣ�����ʵ������IJ��������?��
��4��Fװ�������������?��
�ο��𰸣�
��1��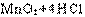 (Ũ)
(Ũ)
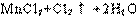 ��2�֣�
��2�֣�
��2������ʳ��ˮ��Ũ���ᣨÿ��1�֣���2�֣�
��3��δ����ȥ��HCl��ˮ������Cl2����D �У�1�֣�����Al��Ӧ������H2��1�֣���H2��Cl2 ��ϻᷢ����ը��1�֣�
��4�����ն������������ֹ��Ⱦ��������ֹ�����е�ˮ��������D�У�2�֣���
�����������
�����Ѷȣ���
3��ʵ���� ijѧ�������ͼ��ʾ��ʵ��װ�ã����������볱ʪ����ʯ�ҷ�Ӧ��ȡ����Ư��(����һ�����ȷ�Ӧ)��
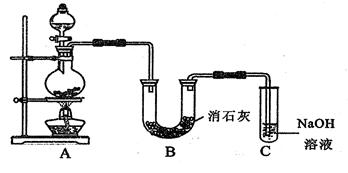
�ݴ˻ش��������⣺
(1) ��Aװ�����ù������������Ũ�����ڼ�����������ȡ���������ڱ�״̬���ռ���33.6L����������������HCl�����ʵ�����?��
(2) Ư�۽���U�ι��в������仯ѧ����ʽ��?��
(3) Cװ�õ�������?��
(4) ��ʵ������Ư�۵���Ч�ɷ�ƫ�͡���ѧ�����������������Ϸ��֣���Ҫԭ������U
�ι��л�������������Ӧ��
���¶Ƚϸ�ʱ��������ʯ�ҷ�Ӧ����Ca(ClO3)2��Ϊ����˸���Ӧ�ķ������ɲ�ȡ�Ĵ�
ʩ��?��
�� ���ж���һ������ӦΪ(�û�ѧ����ʽ��ʾ)?��
Ϊ����˸���Ӧ�ķ������ɽ�װ�����θĽ�?��
(5) ��ͥ��ʹ��Ư��ʱ��Ϊ����ǿƯ���������ɼ���������������(����)
A��ʳ��
B��ʳ��
C���ռ�
D������
�ο��𰸣���14�֣���ÿ�ո�2�֣�
(1) 3mol
(2) 2Cl2+2Ca(OH)2 ="=" CaCl2+Ca(ClO)2+2H2O?
(3) ����δ��Ӧ�����������ֹ��Ⱦ����
(4) �ٽ����ι�������ˮԡ��(����ȴBװ��)
��Ca(OH)2+2HCl ="=" CaCl2+2H2O
��A��B֮������һ��װ�б���ʳ��ˮ��ϴ��ƿ
(5) B
�����������1���ڹ������������Ũ���ᷴӦ�У�MnO2+4HCl MnCl2+Cl2��+H2O��Ũ�����б�������һ�룬�ʱ�������HCl�����ʵ�����3mol��
MnCl2+Cl2��+H2O��Ũ�����б�������һ�룬�ʱ�������HCl�����ʵ�����3mol��
(2) Ư��������������ʯ�ҷ�Ӧ���ɵģ���ѧ����ʽΪ��2Cl2+2Ca(OH)2 ="=" CaCl2+Ca(ClO)2+2H2O��
(3)�����ж���C�е�NaOH��Һ����������������Ӧ�����ն�����������Cװ�õ�����������δ��Ӧ�����������ֹ��Ⱦ������
(4) �ٱ�����¾ͼ�һ������װ�ã��ʿɲ�ȡ�Ĵ�ʩ�ǽ����ι�������ˮԡ��(����ȴBװ��)������A�ӷ������Ȼ�������Ҳ��������ʯ�ҷ�Ӧ���ʷ�Ӧ����ʽ��Ca(OH)2+2HCl ="=" CaCl2+2H2O��Ϊ���ⷴӦ�������ɼ�һ����ȥ�Ȼ��������װ�ã��ʸĽ��Ĵ�ʩ����A��B֮������һ��װ�б���ʳ��ˮ��ϴ��ƿ��
(5)Ư��ֻ������HClO�ž���Ư���ԣ��ʿ��Լ������Ե����ʣ���������HClO����ѡB��
�������������й�ʵ�鷽���ķ�����Ҫ��ѧ����Ϥ��ʵ������ݼ�ԭ�����ܹ�����ͬѧ�ǽ��з������⡢��������������
�����Ѷȣ�һ��
4��ѡ���� ��ˮ������������Ϊ��?��
A����ˮ�к����ȷ���
B����ˮ�к��д��������
C����ˮ�к���������
D����ˮ�к���������
�ο��𰸣�B
�����������
�����Ѷȣ���
5��ѡ���� ������(CN)2���ṹ��N��C��C��N����ѧ������±�ص������ƣ�������������ȷ����
A��(CN)2������C��C���ļ���С��F��F���ļ���
B���軯�ƺ��軯����������ˮ
C��(CN)2�����ԺͲ���������ӳɷ�Ӧ
D��(CN)2��NaOH��Һ��Ӧ������NaCN��NaOCN��H2O
�ο��𰸣�D
���������A������̼ԭ�Ӱ뾶���ڷ�ԭ�Ӱ뾶��(CN)2������C��C���ļ�������F��F���ļ���������B�����������⣬±������������ˮ����AgCN����������ˮ�����軯��Ϊ���Σ�������ˮ������C��±�ص��ʾ��ɺͲ������������ӳɷ�Ӧ��(CN)2Ҳ���ԺͲ���������ӳɷ�Ӧ������D������������±�����ƣ���CN��2����NaOH��Һ��Ӧ��
��CN��2?+2NaOH�TNaCN+NaCNO+H2O����ȷ��
�����Ѷȣ�һ��